Deck 7: Mass Stoichiometry
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال

فتح الحزمة
قم بالتسجيل لفتح البطاقات في هذه المجموعة!
Unlock Deck
Unlock Deck
1/44
العب
ملء الشاشة (f)
Deck 7: Mass Stoichiometry
1
How many molecules of carbon monoxide, CO, comprise 2.34 moles?
A) 1.41 × 1024
B) 2.57 × 1023
C) 1.69 × 1025
D) 2.15 × 1022
A) 1.41 × 1024
B) 2.57 × 1023
C) 1.69 × 1025
D) 2.15 × 1022
1.41 × 1024
2
How many moles of KF are present in 15.2 grams of KF?
A) 0.262
B) 3.82
C) 6.02
D) 882
A) 0.262
B) 3.82
C) 6.02
D) 882
0.262
3
How many moles of CO2 are present in 88.0 grams of CO2?
A) 0.636
B) 1.42
C) 0.88
D) 2.00
A) 0.636
B) 1.42
C) 0.88
D) 2.00
2.00
4
How many atoms are present in a 0.300-mole sample of gold?
A) 4.98 × 1025
B) 1.27 × 1015
C) 1.81 × 1023
D) 6.02 × 1023
A) 4.98 × 1025
B) 1.27 × 1015
C) 1.81 × 1023
D) 6.02 × 1023

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
5
What is the mass of 1.5 × 1021 silicon atoms?
A) 0.0025 g
B) 4.21 × 1022 g
C) 0.070 g
D) 9.52 × 1024 g
A) 0.0025 g
B) 4.21 × 1022 g
C) 0.070 g
D) 9.52 × 1024 g

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
6
A skunk's spray contains the foul-smelling compound butanethiol, C4H8S. What is the percent by mass of sulfur in this compound (to the nearest whole percent)?
A) 8%
B) 36%
C) 55%
D) 75%
A) 8%
B) 36%
C) 55%
D) 75%

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
7
How many atoms are present in a 0.900-mole sample of gold?
A) 1.81 × 1023
B) 1.50 × 1024
C) 5.42 × 1023
D) 6.02 × 1023
A) 1.81 × 1023
B) 1.50 × 1024
C) 5.42 × 1023
D) 6.02 × 1023

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
8
What is the formula mass, to the nearest whole number, for lithium nitrite, LiNO2?
A) 7 amu
B) 44 amu
C) 37 amu
D) 53 amu
A) 7 amu
B) 44 amu
C) 37 amu
D) 53 amu

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
9
How many moles of CO2 are present in 56.0 grams of CO2?
A) 0.786
B) 2.00
C) 0.560
D) 1.27
A) 0.786
B) 2.00
C) 0.560
D) 1.27

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
10
What is the mass of 1.6 × 1021 argon atoms?
A) 0.11 g
B) 0.0027 g
C) 39.4 g
D) 5.11 × 1022 g
A) 0.11 g
B) 0.0027 g
C) 39.4 g
D) 5.11 × 1022 g

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
11
What is the mass of 3.00 moles of CS2?
A) 25.4 g
B) 229 g
C) 0.0394 g
D) 1.81 × 1024 g
A) 25.4 g
B) 229 g
C) 0.0394 g
D) 1.81 × 1024 g

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
12
A skunk's spray contains the foul-smelling compound butanethiol, C4H8S. What is the percent by mass of carbon in this compound (to the nearest whole percent)?
A) 8%
B) 31%
C) 55%
D) 75%
A) 8%
B) 31%
C) 55%
D) 75%

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
13
How many atoms are present in a 0.600-mole sample of gold?
A) 3.61 × 1023
B) 1.18 × 1015
C) 9.97 × 1025
D) 6.02 × 1023
A) 3.61 × 1023
B) 1.18 × 1015
C) 9.97 × 1025
D) 6.02 × 1023

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
14
What is the mass of 2.00 moles of CS2?
A) 38.1 g
B) 152 g
C) 0.0262 g
D) 1.20 × 1024 g
A) 38.1 g
B) 152 g
C) 0.0262 g
D) 1.20 × 1024 g

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
15
What is the formula mass, to the nearest whole number, for sodium nitrite, NaNO2?
A) 23 amu
B) 53 amu
C) 69 amu
D) 83 amu
A) 23 amu
B) 53 amu
C) 69 amu
D) 83 amu

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
16
What is the mass of 3.20 moles of KF?
A) 18.2 g
B) 0.055 g
C) 186 g
D) 1.93 × 1024 g
A) 18.2 g
B) 0.055 g
C) 186 g
D) 1.93 × 1024 g

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
17
What is the formula mass, to the nearest whole number, for potassium nitrite, KNO2?
A) 39 amu
B) 69 amu
C) 85 amu
D) 153 amu
A) 39 amu
B) 69 amu
C) 85 amu
D) 153 amu

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
18
Lithium carbonate, Li2CO3, is commonly used to treat bipolar disorder. What is the percent by mass of carbon in this compound (to the nearest whole percent)?
A) 8%
B) 16%
C) 58%
D) 75%
A) 8%
B) 16%
C) 58%
D) 75%

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
19
How many molecules of carbon dioxide, CO2, comprise 1.22 moles?
A) 7.34 × 1023
B) 4.93 × 1023
C) 2.65 × 1025
D) 1.37 × 1022
A) 7.34 × 1023
B) 4.93 × 1023
C) 2.65 × 1025
D) 1.37 × 1022

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
20
How many molecules of water, H2O, comprise 2.07 moles?
A) 1.25 × 1024
B) 2.91 × 1023
C) 1.08 × 1025
D) 3.34 × 1022
A) 1.25 × 1024
B) 2.91 × 1023
C) 1.08 × 1025
D) 3.34 × 1022

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
21
Consider the following reaction: Fe + Br2 FeBr2
If 44.2 grams of iron react with an excess of bromine gas, what mass of FeBr2 can form?
(FeBr2 = 215.65 g/mol)
A) 171 g
B) 3.67 × 10-3 g
C) 11.4 g
D) 272 g
If 44.2 grams of iron react with an excess of bromine gas, what mass of FeBr2 can form?
(FeBr2 = 215.65 g/mol)
A) 171 g
B) 3.67 × 10-3 g
C) 11.4 g
D) 272 g

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
22
Based on the following balanced equation, how many moles of CO2 will be produced along with 6 moles of water?
CH4 (g) + 2 O2 (g) CO2 (g) + 2 H2O (g)
A) 2
B) 3
C) 4
D) 8
CH4 (g) + 2 O2 (g) CO2 (g) + 2 H2O (g)
A) 2
B) 3
C) 4
D) 8

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
23
In this reaction, BaCO3 is the:
BaCl2 (aq) + Na2CO3 (aq) BaCO3 (s) + 2 NaCl (aq)
A) excess reagent.
B) reactant.
C) dissociated compound.
D) precipitate.
BaCl2 (aq) + Na2CO3 (aq) BaCO3 (s) + 2 NaCl (aq)
A) excess reagent.
B) reactant.
C) dissociated compound.
D) precipitate.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
24
How many molecules of water, H2O, comprise 3.64 grams?
A) 1.22 × 1023
B) 3.95 × 1025
C) 2.98 × 1024
D) 8.22 × 1024
A) 1.22 × 1023
B) 3.95 × 1025
C) 2.98 × 1024
D) 8.22 × 1024

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
25
Based on the following balanced equation, how many moles of SF6 can form from the combination of 6 moles of S and 15 moles of F2?
S + 3 F2 SF6
A) 5
B) 6
C) 15
D) 20
S + 3 F2 SF6
A) 5
B) 6
C) 15
D) 20

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
26
Based on the following balanced equation, how many moles of H2O can form from the reaction of 6 moles of CH4?
CH4 (g) + 2 O2 (g) CO2 (g) + 2 H2O (g)
A) 6
B) 3
C) 12
D) 18
CH4 (g) + 2 O2 (g) CO2 (g) + 2 H2O (g)
A) 6
B) 3
C) 12
D) 18

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
27
In this reaction, the limiting reagent is: 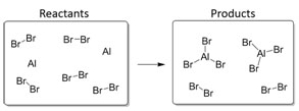
A) Br2.
B) AlBr3.
C) Al.
D) H2O.

A) Br2.
B) AlBr3.
C) Al.
D) H2O.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
28
Consider the following reaction: Fe + Br2 FeBr2
If 38.6 grams of iron react with an excess of bromine gas, what mass of FeBr2 can form?
(FeBr2 = 215.65 g/mol)
A) 149 g
B) 3.20 × 10-3 g
C) 10.0 g
D) 312 g
If 38.6 grams of iron react with an excess of bromine gas, what mass of FeBr2 can form?
(FeBr2 = 215.65 g/mol)
A) 149 g
B) 3.20 × 10-3 g
C) 10.0 g
D) 312 g

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
29
How many molecules of carbon dioxide, CO2, comprise 2.55 grams?
A) 3.49 × 1022
B) 6.76 × 1025
C) 1.04 × 1025
D) 2.86 × 1023
A) 3.49 × 1022
B) 6.76 × 1025
C) 1.04 × 1025
D) 2.86 × 1023

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
30
In this reaction, the symbol (aq) after BaCl2 means that it is:
BaCl2 (aq) + Na2CO3 (aq) BaCO3 (s) + 2 NaCl (aq)
A) the excess reagent.
B) an ionic compound.
C) a reactant.
D) dissolved in water.
BaCl2 (aq) + Na2CO3 (aq) BaCO3 (s) + 2 NaCl (aq)
A) the excess reagent.
B) an ionic compound.
C) a reactant.
D) dissolved in water.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
31
What is the mass of 1.6 × 1021 neon atoms?
A) 0.054 g
B) 0.0027 g
C) 19 g
D) 3.2 × 1022 g
A) 0.054 g
B) 0.0027 g
C) 19 g
D) 3.2 × 1022 g

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
32
Consider the following reaction: 4 Fe + 3 O2 2 Fe2O3
If 44.2 grams of iron react with an excess of oxygen gas, what mass of Fe2O3 can form?
(Fe2O3 = 159.70 g/mol)
A) 63.2 g
B) 253 g
C) 15.5 g
D) 126 g
If 44.2 grams of iron react with an excess of oxygen gas, what mass of Fe2O3 can form?
(Fe2O3 = 159.70 g/mol)
A) 63.2 g
B) 253 g
C) 15.5 g
D) 126 g

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
33
In this reaction, ZnCO3 is the:
ZnBr2 (aq) + K2CO3 (aq) 2 KBr (aq) + ZnCO3 (s)
A) precipitate.
B) reactant.
C) dissociated compound.
D) excess reagent.
ZnBr2 (aq) + K2CO3 (aq) 2 KBr (aq) + ZnCO3 (s)
A) precipitate.
B) reactant.
C) dissociated compound.
D) excess reagent.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
34
Based on the following balanced equation, how many moles of SF6 can form from the combination of 11 moles of S and 18 moles of F2?
S + 3 F2 SF6
A) 6
B) 11
C) 18
D) 29
S + 3 F2 SF6
A) 6
B) 11
C) 18
D) 29

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
35
Based on the following balanced equation, how many moles of SF6 can form from the combination of 5 moles of S and 18 moles of F2?
S + 3 F2 SF6
A) 6
B) 5
C) 18
D) 23
S + 3 F2 SF6
A) 6
B) 5
C) 18
D) 23

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
36
Consider the following reaction: Fe + Br2 FeBr2
If 53.2 grams of iron react with an excess of bromine gas, what mass of FeBr2 can form?
(FeBr2 = 215.65 g/mol)
A) 226 g
B) 13.8 g
C) 205 g
D) 4.41 × 10-3 g
If 53.2 grams of iron react with an excess of bromine gas, what mass of FeBr2 can form?
(FeBr2 = 215.65 g/mol)
A) 226 g
B) 13.8 g
C) 205 g
D) 4.41 × 10-3 g

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
37
How many molecules of carbon monoxide, CO, comprise 4.82 grams?
A) 1.04 × 1023
B) 8.13 × 1025
C) 3.50 × 1024
D) 2.24 × 1022
A) 1.04 × 1023
B) 8.13 × 1025
C) 3.50 × 1024
D) 2.24 × 1022

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
38
In this reaction, the excess reagent is: 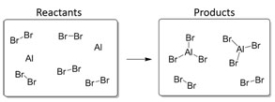
A) Br2.
B) AlBr3.
C) Al.
D) H2O.

A) Br2.
B) AlBr3.
C) Al.
D) H2O.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
39
Based on the following balanced equation, how many moles of O2 will be needed to react completely with of 4 moles of CH4?
CH4 (g) + 2 O2 (g) CO2 (g) + 2 H2O (g)
A) 2
B) 4
C) 8
D) 12
CH4 (g) + 2 O2 (g) CO2 (g) + 2 H2O (g)
A) 2
B) 4
C) 8
D) 12

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
40
In this reaction, the symbol (aq) after ZnBr2 means that it is:
ZnBr2 (aq) + K2CO3 (aq) 2 KBr (aq) + ZnCO3 (s)
A) the excess reagent.
B) an ionic compound.
C) a reactant.
D) dissolved in water.
ZnBr2 (aq) + K2CO3 (aq) 2 KBr (aq) + ZnCO3 (s)
A) the excess reagent.
B) an ionic compound.
C) a reactant.
D) dissolved in water.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
41
Consider the following reaction: 4 Fe + 3 O2 2 Fe2O3
If 44.2 grams of oxygen react with an excess of iron, what mass of Fe2O3 can form?
(Fe2O3 = 159.70 g/mol)
A) 147 g
B) 331 g
C) 294 g
D) 221 g
If 44.2 grams of oxygen react with an excess of iron, what mass of Fe2O3 can form?
(Fe2O3 = 159.70 g/mol)
A) 147 g
B) 331 g
C) 294 g
D) 221 g

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
42
A chemist carries out this reaction in the laboratory using 4.31 grams of zinc and an excess of sulfur: Zn + S ZnS
From the balanced equation, she calculates that she should obtain 6.41 grams of zinc sulfide. However, she isolates only 5.85 grams of product. What is her percent yield for this reaction?
A) 2.1%
B) 67.2%
C) 109.6%
D) 91.3%
From the balanced equation, she calculates that she should obtain 6.41 grams of zinc sulfide. However, she isolates only 5.85 grams of product. What is her percent yield for this reaction?
A) 2.1%
B) 67.2%
C) 109.6%
D) 91.3%

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
43
Consider the following reaction: 4 Fe + 3 O2 2 Fe2O3
How many grams of oxygen gas are needed to react completely with 44.2 grams of iron?
A) 19.0 g
B) 101 g
C) 12.7 g
D) 25.3 g
How many grams of oxygen gas are needed to react completely with 44.2 grams of iron?
A) 19.0 g
B) 101 g
C) 12.7 g
D) 25.3 g

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck
44
A chemist carries out this reaction in the laboratory using 4.31 grams of zinc and an excess of sulfur: Zn + S ZnS
From the balanced equation, she calculates that she should obtain 6.41 grams of zinc sulfide. However, she isolates only 5.01 grams of product. What is her percent yield for this reaction?
A) 67.2%
B) 86.0%
C) 78.2%
D) 128%
From the balanced equation, she calculates that she should obtain 6.41 grams of zinc sulfide. However, she isolates only 5.01 grams of product. What is her percent yield for this reaction?
A) 67.2%
B) 86.0%
C) 78.2%
D) 128%

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 44 في هذه المجموعة.
فتح الحزمة
k this deck








