Deck 15: Aqueous Acidbase Equilibria
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال

فتح الحزمة
قم بالتسجيل لفتح البطاقات في هذه المجموعة!
Unlock Deck
Unlock Deck
1/79
العب
ملء الشاشة (f)
Deck 15: Aqueous Acidbase Equilibria
1
Use the Brønsted-Lowry theory of acids and bases.
Water can act as an acid or a base. Any proton donor and the species generated by removing one of its protons are called a conjugate acid-base pair.
The water autohydrolysis equilibrium exists in any aqueous solution.
Kw [H3O ]eq[OH-]eq 1.0 X10−14 at 25°C in any aqueous solution.
The water autohydrolysis equilibrium exists in any aqueous solution.
Kw [H3O ]eq[OH-]eq 1.0 X10−14 at 25°C in any aqueous solution.
2
Relate pH to concentrations of ions in solution.
pH is a logarithmic scale. A change of 1 pH unit is a 10-fold change of [H3O+(aq)].
3
Calculate concentrations and pH in weak acid and base solutions.
In a solution of a weak acid, only a small fraction of the protons are transferred to the base. In a solution of a weak base, only a small fraction of the protons are transferred from the acid.
4
Recognize and name some common acids and bases.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
5
Calculate the pH of solutions of salts of weak acids or bases.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
6
Explain the factors that contribute to the strength of an acid.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
7
Calculate concentrations in solutions involving multiple equilibria.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
8
A 45.0 mL sample of 0.15 M HCl is added to 38 mL of 0.2 M NaOH. What is the [H3O+] of the resulting solution?
A) 8.5 x 10-4 M
B) 0.010 M
C) 7.6 x 10-3- M
D) 9.8 x 10-13 M
E) 1.02 x 10-14 M
A) 8.5 x 10-4 M
B) 0.010 M
C) 7.6 x 10-3- M
D) 9.8 x 10-13 M
E) 1.02 x 10-14 M

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
9
Identify the acids in the following reaction:H2PO4- + H2O ? H3O+ + HPO42-
A) H2PO4-
B) H3O+
C) H2PO4- and H3O+
D) H2O and H3O+
E) H2O and HPO42-
A) H2PO4-
B) H3O+
C) H2PO4- and H3O+
D) H2O and H3O+
E) H2O and HPO42-

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
10
Identify the bases in the following reaction:H2PO4- + OH- ? H2O + HPO42-
A) H2PO4-
B) OH-
C) H2PO4- and H2O and H3O+
D) OH- and HPO42-
A) H2PO4-
B) OH-
C) H2PO4- and H2O and H3O+
D) OH- and HPO42-

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
11
What is the pH of pure water at 99oC, if Kw (99oC) is 8.836 x 10-13?
A) 7.00
B) -6.02
C) 6.02
D) 12.08
E) 13.88
A) 7.00
B) -6.02
C) 6.02
D) 12.08
E) 13.88

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
12
A 245.0 mL sample of 0.15 M Ba(OH)2 is added to 438 mL of 0.2 M HNO3. What is the pH of the resulting solution?
A) 0.021
B) 1.68
C) 12.32
D) 0.70
E) 13.30
A) 0.021
B) 1.68
C) 12.32
D) 0.70
E) 13.30

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
13
A 0.1 mL sample of 0.01 M HCl is added to 1000 L of water at 298ºK. What is the pH of the resulting solution?
A) 2.0
B) 5.0
C) 7.0
D) 10.0
E) 12.0
A) 2.0
B) 5.0
C) 7.0
D) 10.0
E) 12.0

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
14
A 0.001 mL sample of 0.01 M Ba(OH)2 is added to 1000 L of water at 298ºK. What is the pH of the resulting solution?
A) 2.0
B) 5.0
C) 7.0
D) 10.0
E) 12.0
A) 2.0
B) 5.0
C) 7.0
D) 10.0
E) 12.0

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
15
To have solutions of HCl and acetic acid (CH3CO2H) with the same pH, which of the following needs to be done?
A) The concentration of each solution needs to be the same.
B) The concentration of HCl needs to be higher.
C) The concentration of acetic acid needs to be higher.
D) The solutions can never have the same pH.
E) Volume of acetic acid solution must be lower.
A) The concentration of each solution needs to be the same.
B) The concentration of HCl needs to be higher.
C) The concentration of acetic acid needs to be higher.
D) The solutions can never have the same pH.
E) Volume of acetic acid solution must be lower.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
16
A 1.35 g sample of ammonium chloride is added to sufficient water to give 150.0 mL of solution whose pH is less than 7.0. Several dissociation reactions occur. Which of the following goes essentially to completion?
A) H2O H+ + OH-
B) NH4+ NH3 + H+
C) NH3 NH2- + H+
D) NH4Cl NH4+ + Cl-
E) NH3 + H2O OH- + NH4+
A) H2O H+ + OH-
B) NH4+ NH3 + H+
C) NH3 NH2- + H+
D) NH4Cl NH4+ + Cl-
E) NH3 + H2O OH- + NH4+

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
17
A 1.35 g sample of ammonium chloride is added to sufficient water to give 150.0 mL of solution. Several reactions occur. Which of the following will determine the pH of the solution?
A) 2H2O H3O+ + OH-
B) NH4+ + H2O NH3 + H3O+
C) NH3 + H2O NH2- + H3O+
D) NH4Cl NH4+ + Cl-
E) NH3 + H2O OH- + NH4+
A) 2H2O H3O+ + OH-
B) NH4+ + H2O NH3 + H3O+
C) NH3 + H2O NH2- + H3O+
D) NH4Cl NH4+ + Cl-
E) NH3 + H2O OH- + NH4+

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
18
Identify the major species present in a 0.15 M solution of sodium monohydrogen phosphate, Na2HPO4.
A) Na+, PO43-, H+, H2O
B) Na2HPO4, H2O
C) Na+, H2PO4-, OH-, H2O
D) Na+, HPO42-, H2O
E) Na2HPO4, Na+, HPO42-, H2O
A) Na+, PO43-, H+, H2O
B) Na2HPO4, H2O
C) Na+, H2PO4-, OH-, H2O
D) Na+, HPO42-, H2O
E) Na2HPO4, Na+, HPO42-, H2O

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
19
Which of the following is a weak base?
A) CH3OH
B) KOH
C) CH3CO2H
D) NH4Cl
E) CH3CH2CH2CO2-
A) CH3OH
B) KOH
C) CH3CO2H
D) NH4Cl
E) CH3CH2CH2CO2-

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
20
Which of the following is a weak acid?
A) CH3OH
B) NaOH
C) CH3CO2-
D) NH4Cl
E) CH3CH2CH2CO2CH3
A) CH3OH
B) NaOH
C) CH3CO2-
D) NH4Cl
E) CH3CH2CH2CO2CH3

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
21
Which of the following is a weak base?
A) NaOH
B) CH3CO2H
C) (CH3)2NH
D) KOH
E) HClO2
A) NaOH
B) CH3CO2H
C) (CH3)2NH
D) KOH
E) HClO2

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
22
Which of the following is the conjugate base of the dihydrogenphosphate ion, H2PO4-?
A) H3PO4
B) NaH2PO4
C) OH-
D) HPO42-
E) PO43-
A) H3PO4
B) NaH2PO4
C) OH-
D) HPO42-
E) PO43-

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
23
Which is the conjugate acid of HAsO42-?
A) H3AsO4
B) H3O+
C) OH-
D) H2AsO42-
E) AsO43-
A) H3AsO4
B) H3O+
C) OH-
D) H2AsO42-
E) AsO43-

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
24
The Kas for HClO2, HClO, HIO and HIO3 are 1.1x10-2, 4.0x10-8, 3.2x10-11, and 1.7x10-1, respectively. Which of the following is the strongest base?
A) ClO2-
B) ClO-
C) IO-
D) IO3-
A) ClO2-
B) ClO-
C) IO-
D) IO3-

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
25
A solution of total volume 0.50 L was prepared by the addition of 0.10 moles of KF to sufficient water. From the following, select the major species and the pH of the solution.
A) K+, HF; H O-, H2O, pH = 8.23
B) K+, F-; H+, H2O, pH = 5.76
C) K+, H2O, F-, pH = 8.23
D) K+, H2O, F-, pH = 5.76
E) KF, H3O+, 6.27
A) K+, HF; H O-, H2O, pH = 8.23
B) K+, F-; H+, H2O, pH = 5.76
C) K+, H2O, F-, pH = 8.23
D) K+, H2O, F-, pH = 5.76
E) KF, H3O+, 6.27

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
26
Although you may NOT think of these compounds as being acids, your organic chemistry instructor probably will. Consider the H atoms in bold print in the following compounds.
A= CH3CH2(C=O)CH3
B = CH3CH2(C=O)CH3
C= CH3CH2CH2(C=O)CH3
D= CH3CH2(C=O)CH2(C=O)CH3Select the sequence where the bold H atoms are in order of increasing acidity.
A) D, B, A
B) A, B, D
C) C, B, A
D) A, C, D
E) D, A, C
A= CH3CH2(C=O)CH3
B = CH3CH2(C=O)CH3
C= CH3CH2CH2(C=O)CH3
D= CH3CH2(C=O)CH2(C=O)CH3Select the sequence where the bold H atoms are in order of increasing acidity.
A) D, B, A
B) A, B, D
C) C, B, A
D) A, C, D
E) D, A, C

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
27
Which of the following salt solutions will be the most basic?
A) 0.5 M NaNO3
B) 0.5 M NaNO2
C) 0.75 M NaClO2
D) 0.75 M NaClO4
E) 0.5 M NH4Cl
A) 0.5 M NaNO3
B) 0.5 M NaNO2
C) 0.75 M NaClO2
D) 0.75 M NaClO4
E) 0.5 M NH4Cl

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
28
In the reaction between methyl amine, H2N(CH3) and acetic acid, CH3CO2H, the conjugate acid and base produced are
A) H+ and OH-.
B) H2N(CH3) and CH3CO2H.
C) H3N(CH3)+ and CH3CO2-.
D) H3N(CH3)+ and OH-.
E) H+ and CH3CO2-.
A) H+ and OH-.
B) H2N(CH3) and CH3CO2H.
C) H3N(CH3)+ and CH3CO2-.
D) H3N(CH3)+ and OH-.
E) H+ and CH3CO2-.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
29
When 0.10 moles of HCl are added to 1 L of solution containing 0.12 moles of aqueous Na2CO3, the major species present are
A) Na+, Cl-, H2O, HCO3-.
B) Na+, Cl-, H2O, CO32-.
C) Na+, Cl-, H2O, HCO3-, CO32- .
D) HCl, Na+, CO32-.
E) Na+, Cl-, H2O, H2CO3, CO32.
A) Na+, Cl-, H2O, HCO3-.
B) Na+, Cl-, H2O, CO32-.
C) Na+, Cl-, H2O, HCO3-, CO32- .
D) HCl, Na+, CO32-.
E) Na+, Cl-, H2O, H2CO3, CO32.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
30
Solid NaClO is added to water. What are the major species present?
A) NaClO, HClO and water
B) Na+, Cl-, O2 and water
C) Na+, Cl2, O2- and water
D) Na+, ClO- and water
E) NaClO, Na+, ClO-, water
A) NaClO, HClO and water
B) Na+, Cl-, O2 and water
C) Na+, Cl2, O2- and water
D) Na+, ClO- and water
E) NaClO, Na+, ClO-, water

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
31
What is the pH of a 0.01 M solution of sulphuric acid?
A) 2
B) 1.70
C) 1.85
D) 1.46
E) 12
A) 2
B) 1.70
C) 1.85
D) 1.46
E) 12

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
32
Using the following table, which aqueous 1.0 M solution will have the lowest pH? 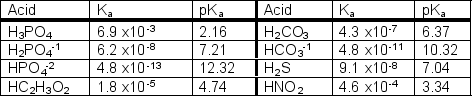
A) Na2CO3
B) NaHS
C) NaC2H3O2
D) NaBr
E) Na3PO4

A) Na2CO3
B) NaHS
C) NaC2H3O2
D) NaBr
E) Na3PO4

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
33
What are the hydronium and hydroxide ion concentrations in a solution of 9.0 M HCl?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
34
If 250 ml of 9.0 M HCl is diluted with 75 ml of water, what is the hydroxide ion concentration of the resulting solution?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
35
What are the hydronium and hydroxide ion concentrations in a solution of 1.00 x10-5 M Ca(OH)2?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
36
What are the hydronium and hydroxide ion concentrations in a solution of 6.4 M NaOH?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
37
At 99°C, the hydronium concentration of pure water is 9.4 x 10-7. Is the solution neutral, acidic, or basic?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
38
A 245.0 mL sample of 0.15 M Ba(OH)2 is added to 438 mL of 0.2 M HNO3. What is the[OH-] of the resulting solution?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
39
What is the pH of an 800 mL solution prepared from 25 g of KOH and water?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
40
What is the pH of a 9 M HCl solution?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
41
What is the pH of a 9 M NaOH solution?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
42
What is the pH of a solution that is 1 x10-10 M in HNO3?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
43
What is the pOH of a solution of 1.00 x10-5 M Ca(OH)2?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
44
What is the [OH-] of a solution whose pH is 7.41?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
45
What is the [H3O+] of a solution whose pOH is 9.45?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
46
What is the [H3O+] of blood whose measured pH = 7.46?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
47
A solution is made by adding 0.1000 mole of the weak acid, HF, to water, and then adding water until the volume of the solution is 1.000 L. Of the acid added, 8.5% is dissociated.
a) What is Ka?
b) What is the pH of the solution?
a) What is Ka?
b) What is the pH of the solution?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
48
Hydroxyl amine, HONH2, is a weak base with Kb of 8.7x10-9. What to extent is a 1.25 molar solution ionized?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
49
Draw a molecular picture that illustrates the reaction that makes solutions of methylamine (CH3NH2) basic.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
50
Draw a molecular picture of the reaction that makes solutions of formic acid acidic.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
51
What is the pH of a 0.600 M HNO2 solution (Ka=5.6 x10-4)?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
52
What is the pH of a 0.0250M CH3NH2 solution (Kb = 4.35 x10-4)?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
53
Determine the % ionized of a 0.200 M solution of lactic acid (pKa = 3.85).

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
54
Determine the Ka of a 0.200 M solution of lactic acid that has a pH = 2.27.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
55
Consider the reaction of monohydrogen carbonate with nitrous acid, HNO2. Write the equation of reaction and identify each conjugate pair of acids and bases.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
56
Consider the reaction of monohydrogen carbonate with ammonia. Write the equation of reaction and identify each conjugate pair of acids and bases.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
57
The conjugate acid of HS-1 is ______ and the conjugate base of H2O is ______.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
58
What is the name for the following acids or bases? 


فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
59
Sodium formate is added to distilled water. Will the resulting solution be acidic, basic or neutral?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
60
Draw a molecular picture that illustrates the reaction responsible for the alkaline nature of sodium phosphate solutions.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
61
Draw a molecular picture that illustrates the reaction responsible for the acidity of solutions of the dimethylammonium ion, (CH3)2NH2+.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
62
If the Kb of IO-(aq) is 3.1x10-4 what is the Ka for hypoiodous acid, HIO?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
63
Solid pyridinium chloride, C5H5NHCl,(5 g) is added to 200 ml of water. What are the major species in solution?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
64
What is the pH of a solution that is prepared by the addition of 15.0 g of NaF to sufficient water to make 1.2 L of solution? (Ka = 6.3 x10-4, pKa = 3.20)

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
65
What is the pH of a 0.15 M solution of NaNO3?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
66
What is the pH of a solution of 20.0 g of NaIO3 in sufficient water to make 988 ml of solution: Ka (Iodic acid, HIO3 = 1.7x10-1)?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
67
Describe what would happen to the pH of a HNO2 solution if some KNO2 was added and explain why.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
68
Which is the strongest acid, HClO4, H ClO3, H ClO2, H ClO and why?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
69
Which is the strongest base, H2PO4-, HPO42- or PO43- and why?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
70
Which acid is a strong acid, HClO4 or HBrO4 and why?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
71
The pKas of the acids, HXO (X= I, Cl, Br) are (in random order) 8.69, 7.53 10.64. Which is the value for HIO?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
72
Which of the group 16 binary hydrides would you expect to be the strongest acid?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
73
Which is a stronger acid, Cl3CCO2H or CH3CO2H and why?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
74
The pKas for the carboxylic acids (CH3CH2CO2H, CH3CO2H, and HCO2H) are (in random order) 3.75, 4.75, 4.87. Place the appropriate pKa with its acid.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
75
Use the following table to answer the questions
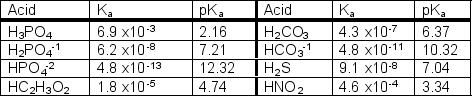
-Write the equilibrium reaction for Kb2 of H3PO4.

-Write the equilibrium reaction for Kb2 of H3PO4.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
76
Use the following table to answer the questions

-Write the equilibrium reaction for Kb2 of H2CO3.

-Write the equilibrium reaction for Kb2 of H2CO3.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
77
Use the following table to answer the questions
![Use the following table to answer the questions -A solution is made by dissolving 0.1 mole Na<sub>3</sub>PO<sub>4</sub> in water, adding HCl and water to give 1.00 L of solution with a pH of 7.60. What is the [HPO<sub>4</sub><sup>-</sup>] in this solution?](https://d2lvgg3v3hfg70.cloudfront.net/TB9687/11ee726d_d43b_942f_827e_4b3e54e216b5_TB9687_00.jpg)
-A solution is made by dissolving 0.1 mole Na3PO4 in water, adding HCl and water to give 1.00 L of solution with a pH of 7.60. What is the [HPO4-] in this solution?
![Use the following table to answer the questions -A solution is made by dissolving 0.1 mole Na<sub>3</sub>PO<sub>4</sub> in water, adding HCl and water to give 1.00 L of solution with a pH of 7.60. What is the [HPO<sub>4</sub><sup>-</sup>] in this solution?](https://d2lvgg3v3hfg70.cloudfront.net/TB9687/11ee726d_d43b_942f_827e_4b3e54e216b5_TB9687_00.jpg)
-A solution is made by dissolving 0.1 mole Na3PO4 in water, adding HCl and water to give 1.00 L of solution with a pH of 7.60. What is the [HPO4-] in this solution?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
78
Use the following table to answer the questions
![Use the following table to answer the questions -A solution is made by dissolving 0.1 mole Na<sub>2</sub>HPO<sub>4</sub> in 1.00 L water. What is the [H<sub>2</sub>PO<sub>4</sub><sup>-</sup>] in this solution?](https://d2lvgg3v3hfg70.cloudfront.net/TB9687/11ee726d_d43b_942f_827e_4b3e54e216b5_TB9687_00.jpg)
-A solution is made by dissolving 0.1 mole Na2HPO4 in 1.00 L water. What is the [H2PO4-] in this solution?
![Use the following table to answer the questions -A solution is made by dissolving 0.1 mole Na<sub>2</sub>HPO<sub>4</sub> in 1.00 L water. What is the [H<sub>2</sub>PO<sub>4</sub><sup>-</sup>] in this solution?](https://d2lvgg3v3hfg70.cloudfront.net/TB9687/11ee726d_d43b_942f_827e_4b3e54e216b5_TB9687_00.jpg)
-A solution is made by dissolving 0.1 mole Na2HPO4 in 1.00 L water. What is the [H2PO4-] in this solution?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck
79
Use the following table to answer the questions

-What will be the dominant phosphate species in a solution when a small amount of H3PO4 is added to a solution whose pH is maintained at pH = 11?

-What will be the dominant phosphate species in a solution when a small amount of H3PO4 is added to a solution whose pH is maintained at pH = 11?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 79 في هذه المجموعة.
فتح الحزمة
k this deck








