Deck 4: Periodic Properties of the Elements
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال

فتح الحزمة
قم بالتسجيل لفتح البطاقات في هذه المجموعة!
Unlock Deck
Unlock Deck
1/145
العب
ملء الشاشة (f)
Deck 4: Periodic Properties of the Elements
1
When filling degenerate orbitals,electrons fill them singly first,with parallel spins is known as
A) Pauli exclusion principle.
B) Hund's rule.
C) Aufbau principle.
D) Heisenberg uncertainty principle.
A) Pauli exclusion principle.
B) Hund's rule.
C) Aufbau principle.
D) Heisenberg uncertainty principle.
Hund's rule.
2
Which of the following elements is a actinide?
A) Ce
B) Na
C) U
D) Ar
E) Rg
A) Ce
B) Na
C) U
D) Ar
E) Rg
U
3
Which of the following statements is TRUE?
A) An orbital that penetrates into the region occupied by core electrons is less shielded from nuclear charge than an orbital that does not penetrate and therefore has a lower energy.
B) An orbital that penetrates into the region occupied by core electrons is more shielded from nuclear charge than an orbital that does not penetrate and therefore has a lower energy.
C) It is possible for two electrons in the same atom to have identical values for all four quantum numbers.
D) Two electrons in the same orbital can have the same spin.
E) None of the above are true.
A) An orbital that penetrates into the region occupied by core electrons is less shielded from nuclear charge than an orbital that does not penetrate and therefore has a lower energy.
B) An orbital that penetrates into the region occupied by core electrons is more shielded from nuclear charge than an orbital that does not penetrate and therefore has a lower energy.
C) It is possible for two electrons in the same atom to have identical values for all four quantum numbers.
D) Two electrons in the same orbital can have the same spin.
E) None of the above are true.
An orbital that penetrates into the region occupied by core electrons is less shielded from nuclear charge than an orbital that does not penetrate and therefore has a lower energy.
4
Predict the charge that an ion formed from sodium would have.
A) 1-
B) 6+
C) 3-
D) 1+
E) 2-
A) 1-
B) 6+
C) 3-
D) 1+
E) 2-

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
5
Which of the following statements is FALSE?
A) Halogens are very reactive elements.
B) The alkali metals are fairly unreactive.
C) Sulfur is a main group element.
D) Noble gases do not usually form ions.
E) Zn is a transition metal.
A) Halogens are very reactive elements.
B) The alkali metals are fairly unreactive.
C) Sulfur is a main group element.
D) Noble gases do not usually form ions.
E) Zn is a transition metal.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
6
Predict the charge that a calcium ion would have.
A) 6-
B) 2-
C) 3+
D) 2+
E) 1+
A) 6-
B) 2-
C) 3+
D) 2+
E) 1+

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
7
Which of the following elements is a lanthanide?
A) Ce
B) Na
C) U
D) Ar
E) Rg
A) Ce
B) Na
C) U
D) Ar
E) Rg

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
8
Only two electrons,with opposing spins,are allowed in each orbital is known as the
A) Pauli exclusion principle.
B) Hund's rule.
C) Aufbau principle.
D) Heisenberg uncertainty principle.
A) Pauli exclusion principle.
B) Hund's rule.
C) Aufbau principle.
D) Heisenberg uncertainty principle.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
9
Identify the green-yellowish gas that is used as a disinfecting agent.
A) chlorine
B) bromine
C) iodine
D) fluorine
A) chlorine
B) bromine
C) iodine
D) fluorine

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
10
Which of the following elements is NOT a metal?
A) Ba
B) Mg
C) Xe
D) Pb
E) Ga
A) Ba
B) Mg
C) Xe
D) Pb
E) Ga

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
11
Which of the following does NOT describe a metal?
A) good conductor of heat
B) good conductor of electricity
C) tends to gain electrons
D) forms ionic compounds with nonmetals
E) found on the left side of the periodic table
A) good conductor of heat
B) good conductor of electricity
C) tends to gain electrons
D) forms ionic compounds with nonmetals
E) found on the left side of the periodic table

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
12
Predict the charge that an aluminum ion would have.
A) 5-
B) 1+
C) 1-
D) 2+
E) 3+
A) 5-
B) 1+
C) 1-
D) 2+
E) 3+

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
13
Predict the charge that an ion formed from sulfur would have.
A) 1-
B) 6+
C) 3-
D) 4+
E) 2-
A) 1-
B) 6+
C) 3-
D) 4+
E) 2-

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
14
No two electrons can have the same four quantum numbers is known as the
A) Pauli exclusion principle.
B) Hund's rule.
C) Aufbau principle.
D) Heisenberg uncertainty principle.
A) Pauli exclusion principle.
B) Hund's rule.
C) Aufbau principle.
D) Heisenberg uncertainty principle.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
15
Semiconductors are
A) metalloids.
B) noble gases.
C) nonmetals.
D) metals.
A) metalloids.
B) noble gases.
C) nonmetals.
D) metals.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
16
Which of the following statements is FALSE?
A) An anion is usually larger than its corresponding atom.
B) Metals tend to form cations.
C) An atoms is usually larger than its corresponding cation.
D) The halogens tend to form 1+ ions.
E) Nonmetals tend to gain electrons.
A) An anion is usually larger than its corresponding atom.
B) Metals tend to form cations.
C) An atoms is usually larger than its corresponding cation.
D) The halogens tend to form 1+ ions.
E) Nonmetals tend to gain electrons.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
17
Which of the following does NOT describe a nonmetal?
A) tend to gain electrons
B) found in the upper right hand corner of the periodic table
C) poor conductor of electricity
D) relatively unreactive
E) poor conductor of heat
A) tend to gain electrons
B) found in the upper right hand corner of the periodic table
C) poor conductor of electricity
D) relatively unreactive
E) poor conductor of heat

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
18
Choose the valence orbital diagram that represents the ground state of Zn.
A)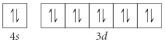
B)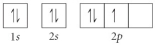
C)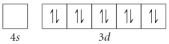
D)
E)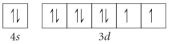
A)

B)

C)

D)

E)


فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
19
Choose the orbital diagram that represents the ground state of N.
A)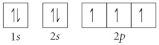
B)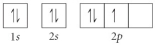
C)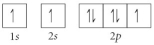
D)
E)
A)

B)

C)

D)

E)


فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
20
The element that corresponds to the electron configuration 1s22s22p63s23p64s13d5 is
A) titanium.
B) vanadium.
C) chromium.
D) manganese.
E) iron.
A) titanium.
B) vanadium.
C) chromium.
D) manganese.
E) iron.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
21
Place the following elements in order of increasing atomic radius. P Ba Cl
A) Ba < P < Cl
B) P < Cl < Ba
C) Cl < P < Ba
D) Cl < Ba < P
E) Ba < Cl < P
A) Ba < P < Cl
B) P < Cl < Ba
C) Cl < P < Ba
D) Cl < Ba < P
E) Ba < Cl < P

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
22
How many valence electrons do the noble gases possess?
A) 1
B) 2
C) 7
D) 6
E) 8
A) 1
B) 2
C) 7
D) 6
E) 8

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
23
Place the following in order of increasing atomic radius. As O Br
A) As < Br < O
B) O < As < Br
C) Br < As < O
D) As < O < Br
E) O < Br < As
A) As < Br < O
B) O < As < Br
C) Br < As < O
D) As < O < Br
E) O < Br < As

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
24
Give the ground state electron configuration for Se.
A) [Ar]4s23d104p4
B) [Ar]4s24d104p4
C) [Ar]4s23d104p6
D) [Ar]4s23d10
E) [Ar]3d104p4
A) [Ar]4s23d104p4
B) [Ar]4s24d104p4
C) [Ar]4s23d104p6
D) [Ar]4s23d10
E) [Ar]3d104p4

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
25
Place the following in order of increasing radius. Br⁻ Na⁺ Rb⁺
A) Br⁻ < Rb⁺ < Na⁺
B) Na⁺ < Rb⁺ < Br⁻
C) Rb⁺ < Br⁻ < Na⁺
D) Br⁻ < Na⁺ < Rb⁺
E) Rb⁺ < Na⁺ < Br⁻
A) Br⁻ < Rb⁺ < Na⁺
B) Na⁺ < Rb⁺ < Br⁻
C) Rb⁺ < Br⁻ < Na⁺
D) Br⁻ < Na⁺ < Rb⁺
E) Rb⁺ < Na⁺ < Br⁻

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
26
Choose the statement that is TRUE.
A) Outer electrons efficiently shield one another from nuclear charge.
B) Core electrons effectively shield outer electrons from nuclear charge.
C) Valence electrons are most difficult of all electrons to remove.
D) Core electrons are the easiest of all electrons to remove.
E) All of the above are true.
A) Outer electrons efficiently shield one another from nuclear charge.
B) Core electrons effectively shield outer electrons from nuclear charge.
C) Valence electrons are most difficult of all electrons to remove.
D) Core electrons are the easiest of all electrons to remove.
E) All of the above are true.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
27
Give the number of valence electrons for Cd.
A) 8
B) 10
C) 12
D) 2
E) 6
A) 8
B) 10
C) 12
D) 2
E) 6

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
28
Give the ground state electron configuration for Cd.
A) [Kr]5s25d10
B) [Kr]5s24d105p2
C) [Kr]4d10
D) [Kr]5s24d8
E) [Kr]5s24d10
A) [Kr]5s25d10
B) [Kr]5s24d105p2
C) [Kr]4d10
D) [Kr]5s24d8
E) [Kr]5s24d10

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
29
Give the ground state electron configuration for I.
A) [Kr]5s24d105p6
B) [Kr]5s24d105p5
C) [Kr]4d105p6
D) [Kr]5s25p6
E) [Kr]5s25d105p6
A) [Kr]5s24d105p6
B) [Kr]5s24d105p5
C) [Kr]4d105p6
D) [Kr]5s25p6
E) [Kr]5s25d105p6

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
30
Identify the element that has a ground state electronic configuration of [Kr]5s24d5.
A) Tc
B) Mn
C) Nb
D) Ru
A) Tc
B) Mn
C) Nb
D) Ru

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
31
How many valence electrons do the halogens possess?
A) 5
B) 6
C) 2
D) 1
E) 7
A) 5
B) 6
C) 2
D) 1
E) 7

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
32
A cation of +2 indicates that an element has
A) lost two electrons.
B) lost two protons.
C) lost two neutrons.
D) gained two electrons.
E) gained two protons.
A) lost two electrons.
B) lost two protons.
C) lost two neutrons.
D) gained two electrons.
E) gained two protons.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
33
How many valence electrons do the alkali metals possess?
A) 1
B) 2
C) 7
D) 6
E) 8
A) 1
B) 2
C) 7
D) 6
E) 8

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
34
Give the ground state electron configuration for Sr.
A) [Kr]5s24d2
B) [Kr]5s24d105p2
C) [Kr]5s2
D) [Kr]5s25d105p2
E) [Kr]5s24d10
A) [Kr]5s24d2
B) [Kr]5s24d105p2
C) [Kr]5s2
D) [Kr]5s25d105p2
E) [Kr]5s24d10

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
35
Place the following in order of decreasing radius. Te2⁻ F⁻ O2⁻
A) F⁻ > O2⁻ > Te2⁻
B) F⁻ > Te2⁻ > O2⁻
C) Te2⁻ > O2⁻ > F⁻
D) Te2⁻ > F⁻ > O2⁻
E) O2⁻ > F⁻ > Te2⁻
A) F⁻ > O2⁻ > Te2⁻
B) F⁻ > Te2⁻ > O2⁻
C) Te2⁻ > O2⁻ > F⁻
D) Te2⁻ > F⁻ > O2⁻
E) O2⁻ > F⁻ > Te2⁻

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
36
How many valence electrons does an atom of Al possess?
A) 1
B) 2
C) 5
D) 3
E) 8
A) 1
B) 2
C) 5
D) 3
E) 8

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
37
How many valence electrons do alkali earth metals possess?
A) 1
B) 2
C) 7
D) 6
E) 8
A) 1
B) 2
C) 7
D) 6
E) 8

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
38
Give the complete electronic configuration for Mn.
A) 1s22s22p63s23p64s24d5
B) 1s22s22p63s23p64s13d6
C) 1s22s22p63s23p64s23d5
D) 1s22s22p63s23p64s24p5
A) 1s22s22p63s23p64s24d5
B) 1s22s22p63s23p64s13d6
C) 1s22s22p63s23p64s23d5
D) 1s22s22p63s23p64s24p5

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
39
Give the ground state electron configuration for Pb.
A) [Xe]6s26p2
B) [Xe]6s25d106p2
C) [Xe]6s25f146d106p2
D) [Xe]6s24f145d106p2
E) [Xe]6s24f145d106s26p2
A) [Xe]6s26p2
B) [Xe]6s25d106p2
C) [Xe]6s25f146d106p2
D) [Xe]6s24f145d106p2
E) [Xe]6s24f145d106s26p2

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
40
Give the number of core electrons for Cd.
A) 44
B) 48
C) 46
D) 45
E) 47
A) 44
B) 48
C) 46
D) 45
E) 47

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
41
Which reaction below represents the first ionization of O?
A) O⁺(g) + e⁻ → O(g)
B) O(g) + e⁻ → O⁻(g)
C) O⁻(g) → O(g) + e⁻
D) O(g) → O⁺(g) + e⁻
E) O⁻(g) + e⁻ → O2⁻(g)
A) O⁺(g) + e⁻ → O(g)
B) O(g) + e⁻ → O⁻(g)
C) O⁻(g) → O(g) + e⁻
D) O(g) → O⁺(g) + e⁻
E) O⁻(g) + e⁻ → O2⁻(g)

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
42
Identify the species that has the smallest radius.
A) N-5
B) N-2
C) N0
D) N+1
E) N+3
A) N-5
B) N-2
C) N0
D) N+1
E) N+3

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
43
Choose the ground state electron configuration for Ti2⁺.
A) [Ar]3d2
B) [Ar]4s2
C) [Ar]4s23d2
D) [Ar]4s23d4
E) [Ar]3d4
A) [Ar]3d2
B) [Ar]4s2
C) [Ar]4s23d2
D) [Ar]4s23d4
E) [Ar]3d4

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
44
Place the following in order of increasing IE1. N F As
A) N < As < F
B) As < N < F
C) F < N < As
D) As < F < N
E) F < As < N
A) N < As < F
B) As < N < F
C) F < N < As
D) As < F < N
E) F < As < N

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
45
Give the ground state electron configuration for Mg2⁺.
A) 1s22s22p63s2
B) 1s22s22p6
C) 1s22s22p63s23p2
D) 1s22s22p63s23p6
E) 1s22s22p63s1
A) 1s22s22p63s2
B) 1s22s22p6
C) 1s22s22p63s23p2
D) 1s22s22p63s23p6
E) 1s22s22p63s1

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
46
Give the ground state electron configuration for Se2⁻.
A) [Ar]4s23d104p4
B) [Ar]4s23d104p2
C) [Ar]4s24p6
D) [Ar]4s23d104p6
E) [Ar]4s23d84p6
A) [Ar]4s23d104p4
B) [Ar]4s23d104p2
C) [Ar]4s24p6
D) [Ar]4s23d104p6
E) [Ar]4s23d84p6

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
47
Which reaction below represents the electron affinity of Li?
A) Li(g) + e⁻ → Li⁻(g)
B) Li(g) → Li⁺(g) + e⁻
C) Li(g) + e⁻ → Li⁺(g)
D) Li⁺(g) → Li(g) + e⁻
E) Li⁺(g) + e⁻ → Li(g)
A) Li(g) + e⁻ → Li⁻(g)
B) Li(g) → Li⁺(g) + e⁻
C) Li(g) + e⁻ → Li⁺(g)
D) Li⁺(g) → Li(g) + e⁻
E) Li⁺(g) + e⁻ → Li(g)

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
48
Give the ground state electron configuration for Rb⁺.
A) [Ar]4s24p6
B) [Kr]5s1
C) [Ar]4s23d104p6
D) [Kr]5s2
E) [Kr]5s24d2
A) [Ar]4s24p6
B) [Kr]5s1
C) [Ar]4s23d104p6
D) [Kr]5s2
E) [Kr]5s24d2

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
49
Choose the valence orbital diagram that represents the ground state of Sr2⁺.
A)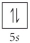
B)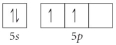
C)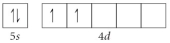
D)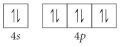
E)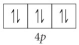
A)

B)

C)

D)

E)


فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
50
Choose the valence orbital diagram that represents the ground state of Se2⁻.
A)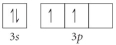
B)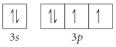
C)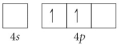
D)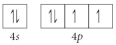
E)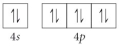
A)

B)

C)

D)

E)


فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
51
Give the ground state electron configuration for Br⁻.
A) [Ar]4s23d104p6
B) [Ar]4s23d104p5
C) [Ar]4s24p6
D) [Ar]4s24d104p6
E) [Ar]4s23d104p4
A) [Ar]4s23d104p6
B) [Ar]4s23d104p5
C) [Ar]4s24p6
D) [Ar]4s24d104p6
E) [Ar]4s23d104p4

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
52
What period 3 element has the following ionization energies (all in kJ/mol)?
IE1 = 1012 IE2 = 1900 IE3= 2910 IE4= 4960 IE5= 6270 IE6 = 22,200
A) Si
B) S
C) P
D) Cl
E) Mg
IE1 = 1012 IE2 = 1900 IE3= 2910 IE4= 4960 IE5= 6270 IE6 = 22,200
A) Si
B) S
C) P
D) Cl
E) Mg

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
53
Give the ground state electron configuration for the ion of Ba.
A) [Kr]5s25p6
B) [Kr]5s24d105p66s26p2
C) [Kr]5s24d105p66s1
D) [Kr]5s24d105p66s2
E) [Kr]5s24d105p6
A) [Kr]5s25p6
B) [Kr]5s24d105p66s26p2
C) [Kr]5s24d105p66s1
D) [Kr]5s24d105p66s2
E) [Kr]5s24d105p6

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
54
Place the following in order of decreasing IE1. Cs Mg Ar
A) Cs > Mg > Ar
B) Mg > Ar > Cs
C) Ar > Mg > Cs
D) Cs > Ar > Mg
E) Mg > Cs > Ar
A) Cs > Mg > Ar
B) Mg > Ar > Cs
C) Ar > Mg > Cs
D) Cs > Ar > Mg
E) Mg > Cs > Ar

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
55
Which reaction below represents the second ionization of Sr?
A) Sr(g) → Sr⁺(g) + e⁻
B) Sr2⁺(g) + e⁻ → Sr⁺(g)
C) Sr⁺(g) + e⁻ → Sr(g)
D) Sr⁻(g) + e⁻ → Sr2⁻(g)
E) Sr⁺(g) → Sr2⁺(g) + e⁻
A) Sr(g) → Sr⁺(g) + e⁻
B) Sr2⁺(g) + e⁻ → Sr⁺(g)
C) Sr⁺(g) + e⁻ → Sr(g)
D) Sr⁻(g) + e⁻ → Sr2⁻(g)
E) Sr⁺(g) → Sr2⁺(g) + e⁻

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
56
Identify the number of valence electrons in Cl-.
A) 6
B) 7
C) 8
D) 5
E) 4
A) 6
B) 7
C) 8
D) 5
E) 4

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
57
Place the following in order of increasing IE1. K Ca Rb
A) Ca < K < Rb
B) Rb < Ca < K
C) Ca < Rb < K
D) Rb < K < Ca
E) K < Ca < Rb
A) Ca < K < Rb
B) Rb < Ca < K
C) Ca < Rb < K
D) Rb < K < Ca
E) K < Ca < Rb

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
58
For a given atom,identify the species that has the smallest radius.
A) cation
B) anion
C) neutral
D) They are all the same size.
A) cation
B) anion
C) neutral
D) They are all the same size.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
59
Choose the ground state electron configuration for Cr3⁺.
A) [Ar]4s13d2
B) [Ar]
C) [Ar]4s23d6
D) [Ar]3d3
E) [Ar]4s23d1
A) [Ar]4s13d2
B) [Ar]
C) [Ar]4s23d6
D) [Ar]3d3
E) [Ar]4s23d1

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
60
Choose the ground state electron configuration for Zn2⁺.
A) [Ar]4s23d8
B) [Ar]3d10
C) [Ar]4s23d6
D) [Ar]
E) [Ar]3d8
A) [Ar]4s23d8
B) [Ar]3d10
C) [Ar]4s23d6
D) [Ar]
E) [Ar]3d8

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
61
Place the following in order of decreasing metallic character. P As K
A) P > As > K
B) As > P > K
C) K > P > As
D) As > K > P
E) K > As > P
A) P > As > K
B) As > P > K
C) K > P > As
D) As > K > P
E) K > As > P

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
62
Describe the reaction of the noble gases with metals.
A) inert
B) vigorous
C) mild reaction
D) forms water
E) dissolves
A) inert
B) vigorous
C) mild reaction
D) forms water
E) dissolves

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
63
Which reaction below represents the second electron affinity of S?
A) S(g) + e⁻ → S⁻(g)
B) S⁻(g) + e⁻ → S2⁻(g)
C) S(g) → S⁺(g) + e⁻
D) S⁻(g) → S(g) + e⁻
E) S2⁻(g) → S⁻(g) + e⁻
A) S(g) + e⁻ → S⁻(g)
B) S⁻(g) + e⁻ → S2⁻(g)
C) S(g) → S⁺(g) + e⁻
D) S⁻(g) → S(g) + e⁻
E) S2⁻(g) → S⁻(g) + e⁻

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
64
Which element has the highest first ionization energy?
A) Cl
B) S
C) I
D) P
E) Ca
A) Cl
B) S
C) I
D) P
E) Ca

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
65
Identify a characteristic of halogens.
A) powerful reducing agents
B) forms water in reactions
C) powerful oxidizing agents
D) absorbs water in reactions
E) inert
A) powerful reducing agents
B) forms water in reactions
C) powerful oxidizing agents
D) absorbs water in reactions
E) inert

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
66
Which species has the highest ionization energy?
A) Mg
B) Mg+
C) Mg2+
D) Al+
E) Al2+
A) Mg
B) Mg+
C) Mg2+
D) Al+
E) Al2+

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
67
Which describes the valance electrons of magnesium?
A) 3s0
B) 3s1
C) 3s2
D) 3s2d1
E) 3s2d2
A) 3s0
B) 3s1
C) 3s2
D) 3s2d1
E) 3s2d2

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
68
Halogens can react with each other to form
A) covalent bonds.
B) ionic bonds.
C) salts.
D) hydrogen halides.
E) metal halides.
A) covalent bonds.
B) ionic bonds.
C) salts.
D) hydrogen halides.
E) metal halides.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
69
Give the complete electronic configuration for Br-.
A) 1s22s22p63s23p64s24p6
B) 1s22s22p63s23p64s24d104p6
C) 1s22s22p63s23p64s23d104p6
D) 1s22s22p63s23p64s23d104p5
E) 1s22s2p63s2p64s23d104p6
A) 1s22s22p63s23p64s24p6
B) 1s22s22p63s23p64s24d104p6
C) 1s22s22p63s23p64s23d104p6
D) 1s22s22p63s23p64s23d104p5
E) 1s22s2p63s2p64s23d104p6

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
70
Give the complete electronic configuration for Ca2+.
A) 1s22s22p63s24p6
B) 1s22s22p63s23p6
C) 1s22s22p63s23p5
D) 1s22s23p64s25p6
E) 1s22s2p63s2p6
A) 1s22s22p63s24p6
B) 1s22s22p63s23p6
C) 1s22s22p63s23p5
D) 1s22s23p64s25p6
E) 1s22s2p63s2p6

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
71
The ________ is a change in energy associated with gaining an electron in the gaseous state for an atom or ion.
A) first ionization energy
B) electron affinity
C) binding energy
D) metallic nature
E) shielding
A) first ionization energy
B) electron affinity
C) binding energy
D) metallic nature
E) shielding

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
72
Place the following in order of increasing metallic character. Rb Cs K Na
A) K < Cs < Na < Rb
B) Na < K < Rb < Cs
C) Cs < Rb < K < Na
D) K < Cs < Rb < Na
E) Na < Rb < Cs < K
A) K < Cs < Na < Rb
B) Na < K < Rb < Cs
C) Cs < Rb < K < Na
D) K < Cs < Rb < Na
E) Na < Rb < Cs < K

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
73
Which ion has the largest radius?
A) Na+
B) Ga3+
C) K+
D) Mg2+
E) Ca2+
A) Na+
B) Ga3+
C) K+
D) Mg2+
E) Ca2+

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
74
Which element would most likely form an ion with a charge of -2?
A) Te
B) I
C) N
D) Na
E) Al
A) Te
B) I
C) N
D) Na
E) Al

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
75
According to Hund's Rule
A) electrons pair off first, then fill orbitals.
B) electrons fill orbitals of the same energy singly and pair up only after the orbitals are all half filled.
C) orbitals of the same energy level have the same energy.
D) no two electrons in the same atom can have the same four quantum numbers.
E) electrons found in the same orbital must have the same spin.
A) electrons pair off first, then fill orbitals.
B) electrons fill orbitals of the same energy singly and pair up only after the orbitals are all half filled.
C) orbitals of the same energy level have the same energy.
D) no two electrons in the same atom can have the same four quantum numbers.
E) electrons found in the same orbital must have the same spin.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
76
Describe the reaction of the alkali metals with non-metals.
A) inert
B) vigorous
C) mild reaction
D) forms water
E) dissolves
A) inert
B) vigorous
C) mild reaction
D) forms water
E) dissolves

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
77
Why does an electron found in a 2s orbital have a lower energy than an electron found in a 2p orbital in multielectron systems?
A) Electrons in the 2s orbital are shielded by electrons in the 2p.
B) There are more nodes found in the 2s orbital.
C) Electrons in the 2s orbital can penetrate the 1s orbital and be closer to the nucleus.
D) The larger number of electrons found in the 2p orbital leads to greater repulsion.
E) The shape of the orbital ultimately determines the energy of the electrons.
A) Electrons in the 2s orbital are shielded by electrons in the 2p.
B) There are more nodes found in the 2s orbital.
C) Electrons in the 2s orbital can penetrate the 1s orbital and be closer to the nucleus.
D) The larger number of electrons found in the 2p orbital leads to greater repulsion.
E) The shape of the orbital ultimately determines the energy of the electrons.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
78
The Pauli Exclusion Principle states that
A) s orbitals are always lower in energy than p orbitals.
B) electrons spin around the nucleus.
C) you can never know the precise position and energy of an electron.
D) The potential energy of two charges particles depends on their distance.
E) no two electrons in the same atom can have the same four quantum numbers.
A) s orbitals are always lower in energy than p orbitals.
B) electrons spin around the nucleus.
C) you can never know the precise position and energy of an electron.
D) The potential energy of two charges particles depends on their distance.
E) no two electrons in the same atom can have the same four quantum numbers.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
79
Which element is diamagnetic?
A) Li
B) F
C) Rb
D) V
E) Zn
A) Li
B) F
C) Rb
D) V
E) Zn

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck
80
Identify the alkali metal that is most reactive with water.
A) Cs
B) Rb
C) K
D) Na
E) Li
A) Cs
B) Rb
C) K
D) Na
E) Li

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 145 في هذه المجموعة.
فتح الحزمة
k this deck








