Deck 7: Quantum Theory and the Electronic Structure of Atoms
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال

فتح الحزمة
قم بالتسجيل لفتح البطاقات في هذه المجموعة!
Unlock Deck
Unlock Deck
1/115
العب
ملء الشاشة (f)
Deck 7: Quantum Theory and the Electronic Structure of Atoms
1
What is the energy in joules of a mole of photons associated with red light of wavelength 7.00 * 102 nm?
A)256 kJ
B)1.71 * 105 J
C)4.72 * 10-43 J
D)12.4 kJ
E)2.12 * 1042 J
A)256 kJ
B)1.71 * 105 J
C)4.72 * 10-43 J
D)12.4 kJ
E)2.12 * 1042 J
1.71 * 105 J
2
Calculate the frequency of visible light having a wavelength of 686 nm.
A)4.37 * 1014 /s
B)4.37 * 105 /s
C)6.17 * 1014 /s
D)2.29 * 10-15 /s
E)2.29 * 10-6 /s
A)4.37 * 1014 /s
B)4.37 * 105 /s
C)6.17 * 1014 /s
D)2.29 * 10-15 /s
E)2.29 * 10-6 /s
4.37 * 1014 /s
3
What is the binding energy (in J/mol or kJ/mol)of an electron in a metal whose threshold frequency for photoelectrons is 2.50 * 1014 /s?
A)99.7 kJ/mol
B)1.66 * 10-19 J/mol
C)2.75 * 10-43 J/mol
D)7.22 * 1017 kJ/mol
E)1.20 * 10-6 J/mol
A)99.7 kJ/mol
B)1.66 * 10-19 J/mol
C)2.75 * 10-43 J/mol
D)7.22 * 1017 kJ/mol
E)1.20 * 10-6 J/mol
99.7 kJ/mol
4
Calculate the wavelength, in nanometers, of the light emitted by a hydrogen atom when its electron falls from the n = 7 to the n = 4 principal energy level. Recall that the energy levels of the H atom are given by En = -2.18 * 10-18 J(1/n2)
A)4.45 * 10-20 nm
B)2.16 * 10-6 nm
C)9.18 * 10-20 nm
D)1.38 * 1014 nm
E)2.16 * 103 nm
A)4.45 * 10-20 nm
B)2.16 * 10-6 nm
C)9.18 * 10-20 nm
D)1.38 * 1014 nm
E)2.16 * 103 nm

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
5
Calculate the wavelength of the light emitted by a hydrogen atom during a transition of its electron from the n = 4 to the n = 1 principal energy level. Recall that for hydrogen En = -2.18 * 10-18 J(1/n2)
A)97.2 nm
B)82.6 nm
C)365 nm
D)0.612 nm
E)6.8 * 10-18 nm
A)97.2 nm
B)82.6 nm
C)365 nm
D)0.612 nm
E)6.8 * 10-18 nm

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
6
Complete this sentence: Atoms emit visible and ultraviolet light
A)as electrons jump from lower energy levels to higher levels.
B)as the atoms condense from a gas to a liquid.
C)as electrons jump from higher energy levels to lower levels.
D)as they are heated and the solid melts to form a liquid.
E)as the electrons move about the atom within an orbit.
A)as electrons jump from lower energy levels to higher levels.
B)as the atoms condense from a gas to a liquid.
C)as electrons jump from higher energy levels to lower levels.
D)as they are heated and the solid melts to form a liquid.
E)as the electrons move about the atom within an orbit.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
7
Calculate the frequency of the light emitted by a hydrogen atom during a transition of its electron from the n = 6 to the n = 3 principal energy level. Recall that for hydrogen En = -2.18 * 10-18 J(1/n2).
A)1.64 * 1015 /s
B)9.13 * 1013 /s
C)3.65 * 1014 /s
D)1.82 * 10-19 /s
E)2.74 * 1014/s
A)1.64 * 1015 /s
B)9.13 * 1013 /s
C)3.65 * 1014 /s
D)1.82 * 10-19 /s
E)2.74 * 1014/s

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
8
What is the wavelength of radiation that has a frequency of 5.39 * 1014 s-1? (c = 2.9979 * 108 m/s)
A)1.80 * 10-3 nm
B)556 nm
C)618 nm
D)6180 nm
E)1.61 * 1023 nm
A)1.80 * 10-3 nm
B)556 nm
C)618 nm
D)6180 nm
E)1.61 * 1023 nm

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
9
In the following diagram of a wave 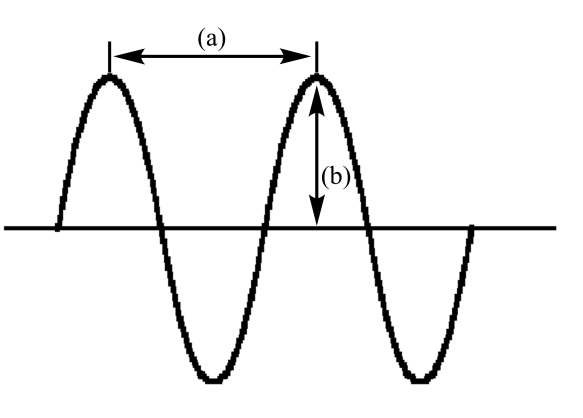
A)(a)is amplitude and (b)is wavelength
B)(a)is frequency and (b)is amplitude
C)(a)is wavelength and (b)is frequency
D)(a)is amplitude and (b)is frequency
E)(a)is wavelength and (b)is amplitude

A)(a)is amplitude and (b)is wavelength
B)(a)is frequency and (b)is amplitude
C)(a)is wavelength and (b)is frequency
D)(a)is amplitude and (b)is frequency
E)(a)is wavelength and (b)is amplitude

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
10
If a hydrogen atom and a helium atom are traveling at the same speed,
A)the wavelength of the hydrogen atom will be about 4 times longer than the wavelength of the helium atom.
B)the wavelength of the hydrogen atom will be about 2 times longer than the wavelength of the helium.
C)the wavelength of the hydrogen atom will be roughly equal to the wavelength of the helium atom.
D)the wavelength of the helium atom will be about 2 times longer than the wavelength of the hydrogen atom.
E)the wavelength of the helium atom will be about 4 times longer than the wavelength of the hydrogen atom.
A)the wavelength of the hydrogen atom will be about 4 times longer than the wavelength of the helium atom.
B)the wavelength of the hydrogen atom will be about 2 times longer than the wavelength of the helium.
C)the wavelength of the hydrogen atom will be roughly equal to the wavelength of the helium atom.
D)the wavelength of the helium atom will be about 2 times longer than the wavelength of the hydrogen atom.
E)the wavelength of the helium atom will be about 4 times longer than the wavelength of the hydrogen atom.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
11
Calculate the frequency of the light emitted by a hydrogen atom during a transition of its electron from the n = 4 to the n = 1 principal energy level. Recall that for hydrogen En = -2.18 *10 -18 J(1/n2)
A)3.08 * 1015 /s
B)1.03 * 108 /s
C)2.06 * 1014 /s
D)1.35 * 10-51 /s
E)8.22 * 1014 /s
A)3.08 * 1015 /s
B)1.03 * 108 /s
C)2.06 * 1014 /s
D)1.35 * 10-51 /s
E)8.22 * 1014 /s

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
12
As the frequency of an electromagnetic wave increases
A)its speed must increase.
B)its wavelength must increase.
C)its amplitude must increase.
D)its energy must increase.
A)its speed must increase.
B)its wavelength must increase.
C)its amplitude must increase.
D)its energy must increase.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
13
What is the energy in joules of a mole of photons associated with visible light of wavelength 486 nm?
A)6.46 * 10-16 J
B)6.46 * 10-25 J
C)2.46 *10-4 J
D)12.4 kJ
E)246 kJ
A)6.46 * 10-16 J
B)6.46 * 10-25 J
C)2.46 *10-4 J
D)12.4 kJ
E)246 kJ

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
14
The second line of the Balmer series occurs at a wavelength of 486.1 nm. What is the energy difference between the initial and final levels of the hydrogen atom in this emission process?
A)2.44 * 1018 J
B)4.09 * 10-19 J
C)4.09 * 10-22 J
D)4.09 * 10-28 J
E)1.07 * 10-48 J
A)2.44 * 1018 J
B)4.09 * 10-19 J
C)4.09 * 10-22 J
D)4.09 * 10-28 J
E)1.07 * 10-48 J

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
15
What is the energy in joules of one photon of microwave radiation with a wavelength 0.122 m? (c = 2.9979 * 108 m/s; h = 6.626 * 10-34 J0s)
A)2.70 * 10-43 J
B)5.43 * 10-33 J
C)1.63 * 10-24 J
D)4.07 * 10-10 J
E)2.46 * 109 J
A)2.70 * 10-43 J
B)5.43 * 10-33 J
C)1.63 * 10-24 J
D)4.07 * 10-10 J
E)2.46 * 109 J

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
16
Calculate the frequency of visible light having a wavelength of 486 nm.
A)2.06 * 1014 /s
B)2.06 * 106 /s
C)6.17 * 1014 /s
D)1.20 * 10-15 /s
E)4.86 * 10-7 /s
A)2.06 * 1014 /s
B)2.06 * 106 /s
C)6.17 * 1014 /s
D)1.20 * 10-15 /s
E)4.86 * 10-7 /s

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
17
A proton is roughly 1800 times more massive than an electron.If a proton and an electron are traveling at the same speed,
A)the wavelength of the photon will be about 1800 times longer than the wavelength of the electron.
B)the wavelength of the photon will be about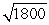 times longer than the wavelength of the electron.
times longer than the wavelength of the electron.
C)the wavelength of the photon will be roughly equal to the wavelength of the electron.
D)the wavelength of the electron will be about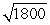 times longer than the wavelength of the photon.
times longer than the wavelength of the photon.
E)the wavelength of the electron will be about 1800 times longer than the wavelength of the photon.
A)the wavelength of the photon will be about 1800 times longer than the wavelength of the electron.
B)the wavelength of the photon will be about
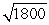 times longer than the wavelength of the electron.
times longer than the wavelength of the electron.C)the wavelength of the photon will be roughly equal to the wavelength of the electron.
D)the wavelength of the electron will be about
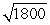 times longer than the wavelength of the photon.
times longer than the wavelength of the photon.E)the wavelength of the electron will be about 1800 times longer than the wavelength of the photon.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
18
A photon is roughly 1800 times more massive than an electron.If a proton and an electron have the same kinetic energy,
A)the wavelength of the photon will be about 1800 times longer than the wavelength of the electron.
B)the wavelength of the photon will be about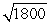 times longer than the wavelength of the electron.
times longer than the wavelength of the electron.
C)the wavelength of the photon will be roughly equal to the wavelength of the electron.
D)the wavelength of the electron will be about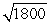 times longer than the wavelength of the photon.
times longer than the wavelength of the photon.
E)the wavelength of the electron will be about 1800 times longer than the wavelength of the photon.
A)the wavelength of the photon will be about 1800 times longer than the wavelength of the electron.
B)the wavelength of the photon will be about
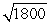 times longer than the wavelength of the electron.
times longer than the wavelength of the electron.C)the wavelength of the photon will be roughly equal to the wavelength of the electron.
D)the wavelength of the electron will be about
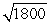 times longer than the wavelength of the photon.
times longer than the wavelength of the photon.E)the wavelength of the electron will be about 1800 times longer than the wavelength of the photon.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
19
Calculate the energy, in joules, required to excite a hydrogen atom by causing an electronic transition from the n = 1 to the n = 4 principal energy level. Recall that the energy levels of the H atom are given by En = -2.18 * 10-18 J(1/n2)
A)2.07 * 10-29 J
B)2.19 * 105 J
C)2.04 *10-18 J
D)3.27 * 10-17 J
E)2.25 * 10-18 J
A)2.07 * 10-29 J
B)2.19 * 105 J
C)2.04 *10-18 J
D)3.27 * 10-17 J
E)2.25 * 10-18 J

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
20
What is the wavelength of radiation that has a frequency of 2.10 *1014 s -1?
A)6.30 * 1022 m
B)7.00 * 102 nm
C)7.00 * 105 m
D)1.43 * 10-6 m
E)3.00 * 108 m
A)6.30 * 1022 m
B)7.00 * 102 nm
C)7.00 * 105 m
D)1.43 * 10-6 m
E)3.00 * 108 m

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
21
A possible set of quantum numbers for the last electron added to complete an atom of gallium (Ga)in its ground state is 


فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
22
How many orbitals are allowed in a subshell if the angular momentum quantum number for electrons in that subshell is 3?
A)1
B)3
C)5
D)7
E)9
A)1
B)3
C)5
D)7
E)9

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
23
The maximum number of electrons that can occupy an energy level described by the principal quantum number, n, is
A)n
B)n + 1
C)2n
D)2n2
E)n2
A)n
B)n + 1
C)2n
D)2n2
E)n2

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
24
Calculate the wavelength associated with a 20Ne+ ion moving at a velocity of 2.0 * 105 m/s.The atomic mass of Ne-20 is 19.992 amu.
A)1.0 * 10-13 m
B)1.0 * 10-16 m
C)1.0 * 10-18 m
D)9.7 * 1012 m
E)2.0 * 10-13 cm
A)1.0 * 10-13 m
B)1.0 * 10-16 m
C)1.0 * 10-18 m
D)9.7 * 1012 m
E)2.0 * 10-13 cm

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
25
Which one of the following sets of quantum numbers is not possible? 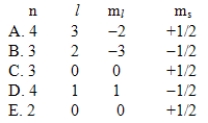
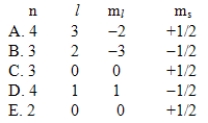

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
26
Electrons in an orbital with l = 3 are in a/an
A)d orbital.
B)f orbital.
C)g orbital.
D)p orbital.
E)s orbital.
A)d orbital.
B)f orbital.
C)g orbital.
D)p orbital.
E)s orbital.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
27
In an electron microscope, electrons are accelerated to great velocities. Calculate the wavelength of an electron traveling with a velocity of 7.0 * 103 kilometers per second. The mass of an electron is 9.1 * 10-28 g.
A)1.0 * 10-13 m
B)1.0 * 10-7 m
C)1.0 m
D)1.0 * 10-10 m
A)1.0 * 10-13 m
B)1.0 * 10-7 m
C)1.0 m
D)1.0 * 10-10 m

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
28
The longest wavelength of light that causes electrons to be ejected from the surface of a copper plate is 243 nm. What is the maximum velocity of the electrons ejected when light of wavelength 200.nm shines on a copper plate?
A)1.48 * 106 m/s
B)6.22 * 105 m/s
C)4.67 * 104 m/s
D)1.97 * 104 m/s
E)1.34 * 106 m/s
A)1.48 * 106 m/s
B)6.22 * 105 m/s
C)4.67 * 104 m/s
D)1.97 * 104 m/s
E)1.34 * 106 m/s

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
29
If a hydrogen atom and a helium atom have the same kinetic energy,
A)the wavelength of the hydrogen atom will be about 4 times longer than the wavelength of the helium atom.
B)the wavelength of the hydrogen atom will be about 2 times longer than the wavelength of the helium.
C)the wavelength of the hydrogen atom will be roughly equal to the wavelength of the helium atom.
D)the wavelength of the helium atom will be about 2 times longer than the wavelength of the hydrogen atom.
E)the wavelength of the helium atom will be about 4 times longer than the wavelength of the hydrogen atom.
A)the wavelength of the hydrogen atom will be about 4 times longer than the wavelength of the helium atom.
B)the wavelength of the hydrogen atom will be about 2 times longer than the wavelength of the helium.
C)the wavelength of the hydrogen atom will be roughly equal to the wavelength of the helium atom.
D)the wavelength of the helium atom will be about 2 times longer than the wavelength of the hydrogen atom.
E)the wavelength of the helium atom will be about 4 times longer than the wavelength of the hydrogen atom.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
30
"No two electrons in an atom can have the same four quantum numbers" is a statement of
A)the Pauli exclusion principle.
B)Bohr's equation.
C)Hund's rule.
D)de Broglie's relation.
E)Dalton's atomic theory.
A)the Pauli exclusion principle.
B)Bohr's equation.
C)Hund's rule.
D)de Broglie's relation.
E)Dalton's atomic theory.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
31
A single pulse of a laser yields an average of 5.00 * 1018 photons with = 633 nm. If melting ice to water at 0°C requires 6.01 kJ/mol, what is the fewest number of laser pulses need to melt 10.0 g of ice?
A)3830
B)3340
C)38300
D)2120
E)212
A)3830
B)3340
C)38300
D)2120
E)212

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
32
A common way of initiating certain chemical reactions with light involves the generation of free halogen atoms in solution. If H for the reaction Cl2(g) 2Cl(g)is 242.8 kJ/mol, what is the longest wavelength of light that will produce free chlorine atoms in solution?
A)246.3 nm
B)465.2 nm
C)349.3 nm
D)698.6 nm
E)492.6 nm
A)246.3 nm
B)465.2 nm
C)349.3 nm
D)698.6 nm
E)492.6 nm

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
33
When photons with a wavelength of 310.nm strike a magnesium plate, the maximum velocity of the ejected electrons is 3.45 * 105 m/s. Calculate the binding energy of electrons to the magnesium surface.
A)386 kJ/mol
B)419 kJ/mol
C)32.7 kJ/mol
D)321 kJ/mol
E)353 kJ/mol
A)386 kJ/mol
B)419 kJ/mol
C)32.7 kJ/mol
D)321 kJ/mol
E)353 kJ/mol

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
34
The number of orbitals in a d subshell is
A)1
B)2
C)3
D)5
E)7
A)1
B)2
C)3
D)5
E)7

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
35
Electrons can be used to probe the arrangement of atoms on a solid surface if the wavelength of the electrons is comparable with the spacing between the atoms. Which of the following electron velocities would be appropriate for use in this application if the atoms are separated by 0.320 nm?
A)2.27 * 106 m/s
B)1.24 * 103 m/s
C)3.00 * 108 m/s
D)4.41 * 106 m/s
E)8.06 * 103 m/s
A)2.27 * 106 m/s
B)1.24 * 103 m/s
C)3.00 * 108 m/s
D)4.41 * 106 m/s
E)8.06 * 103 m/s

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
36
A possible set of quantum numbers for the last electron added to complete an atom of germanium (Ge)in its ground state is 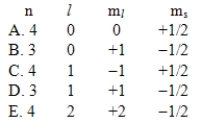


فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
37
Calculate the wavelength of a neutron that has a velocity of 250 cm/s. (The mass of a neutron = 1.675 * 10-24 g; h = 6.626 * 10-34 J.s)
A)16 pm
B)0.016 nm
C)0.16 nm
D)160 nm
E)1.6 * 10-4 m
A)16 pm
B)0.016 nm
C)0.16 nm
D)160 nm
E)1.6 * 10-4 m

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
38
Which one of the following sets of quantum numbers is not possible? 


فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
39
What is the maximum number of electrons in an atom that can have the following set of quantum numbers? n = 4 l = 3 ml = -2 ms = +1/2
A)0
B)1
C)2
D)6
E)10
A)0
B)1
C)2
D)6
E)10

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
40
The orbital diagram for a ground-state nitrogen atom is 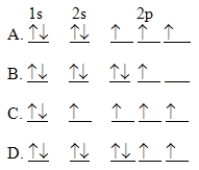


فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
41
Which of the following is the ground-state electron configuration of a calcium atom?
A)[Ne]3s2
B)[Ne]3s23p6
C)[Ar]4s13d1
D)[Ar]4s2
E)[Ar]3d2
A)[Ne]3s2
B)[Ne]3s23p6
C)[Ar]4s13d1
D)[Ar]4s2
E)[Ar]3d2

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
42
The orbital diagram for a ground-state oxygen atom is 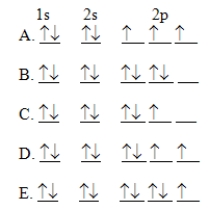


فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
43
Which ground-state atom has an electron configuration described by the following orbital diagram? 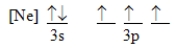
A)phosphorus
B)nitrogen
C)arsenic
D)vanadium
E)none of these
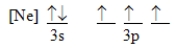
A)phosphorus
B)nitrogen
C)arsenic
D)vanadium
E)none of these

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
44
A ground-state atom of manganese has ___ unpaired electrons and is _____.
A)0, diamagnetic
B)2, diamagnetic
C)3, paramagnetic
D)5, paramagnetic
E)7, paramagnetic
A)0, diamagnetic
B)2, diamagnetic
C)3, paramagnetic
D)5, paramagnetic
E)7, paramagnetic

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
45
Which element has the following ground-state electron configuration? [Kr]5s24d105p3
A)Sn
B)Sb
C)Pb
D)Bi
E)Te
A)Sn
B)Sb
C)Pb
D)Bi
E)Te

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
46
How many unpaired electrons does a ground-state atom of sulfur have?
A)0
B)1
C)2
D)3
E)4
A)0
B)1
C)2
D)3
E)4

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
47
Which element has the following ground-state electron configuration? [Ar]4s23d104p5
A)aresnic
B)bromine
C)iodine
D)selenium
E)tellerium
A)aresnic
B)bromine
C)iodine
D)selenium
E)tellerium

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
48
Which element has the following ground-state electron configuration? [Kr]5s14d5
A)Mn
B)Mo
C)Nb
D)Re
E)Tc
A)Mn
B)Mo
C)Nb
D)Re
E)Tc

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
49
Which element has the following ground-state electron configuration? [Kr]5s24d105p2
A)Sn
B)Sb
C)Pb
D)Ge
E)Te
A)Sn
B)Sb
C)Pb
D)Ge
E)Te

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
50
Which element has the following ground-state electron configuration? 1s22s22p63s2
A)Na
B)Mg
C)Al
D)Si
E)Ne
A)Na
B)Mg
C)Al
D)Si
E)Ne

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
51
How many electrons are there in the 2nd principal energy level (n = 2)of a phosphorus atom?
A)3
B)5
C)6
D)8
E)10
A)3
B)5
C)6
D)8
E)10

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
52
The orbital diagram for a ground state carbon atom is 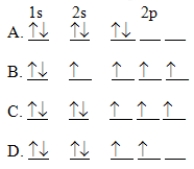


فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
53
The electron configuration of a ground-state copper atom is
A)[Ar]4s24d4
B)[Ar]4s24p63d3
C)[Ar]4s23d9
D)[Ar]3d9
E)[Ar]4s13d10
A)[Ar]4s24d4
B)[Ar]4s24p63d3
C)[Ar]4s23d9
D)[Ar]3d9
E)[Ar]4s13d10

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
54
Which ground-state atom has an electron configuration described by the following orbital diagram? 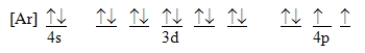
A)phosphorus
B)germanium
C)selenium
D)tellurium
E)none of these

A)phosphorus
B)germanium
C)selenium
D)tellurium
E)none of these

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
55
A ground-state atom of arsenic has
A)no unpaired electrons.
B)one unpaired electron.
C)two unpaired electrons.
D)three unpaired electrons.
E)four unpaired electrons.
A)no unpaired electrons.
B)one unpaired electron.
C)two unpaired electrons.
D)three unpaired electrons.
E)four unpaired electrons.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
56
The electron configuration of a ground-state Co atom is
A)[Ar]4s23d7
B)1s22s22p63s23d9
C)[Ne]3s23d7
D)[Ar]4s13d5
E)[Ar]4s24d7
A)[Ar]4s23d7
B)1s22s22p63s23d9
C)[Ne]3s23d7
D)[Ar]4s13d5
E)[Ar]4s24d7

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
57
How many electrons are there in the 3rd principal energy level (n = 3)of a phosphorus atom?
A)3
B)5.
C)6
D)8
E)10
A)3
B)5.
C)6
D)8
E)10

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
58
The electron configuration of a ground-state vanadium atom is
A)[Ar]4s24d3
B)[Ar]4s24p3
C)[Ar]4s23d3
D)[Ar]3d5
A)[Ar]4s24d3
B)[Ar]4s24p3
C)[Ar]4s23d3
D)[Ar]3d5

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
59
The ground-state electron configuration for an atom of indium is
A)[Kr]5s24p64d5
B)[Ar]4s23d104p1
C)[Ar]4s24p63d5
D)[Kr]5s25p64d5
E)[Kr]5s24d105p1
A)[Kr]5s24p64d5
B)[Ar]4s23d104p1
C)[Ar]4s24p63d5
D)[Kr]5s25p64d5
E)[Kr]5s24d105p1

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
60
Which ground-state atom has an electron configuration described by the following orbital diagram? 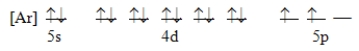
A)antimony
B)germanium
C)indium
D)lead
E)tin
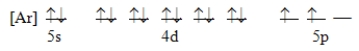
A)antimony
B)germanium
C)indium
D)lead
E)tin

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
61
Which choice lists two elements with ground-state electron configurations that are well known exceptions to the Aufbau principle?
A)Cu and C
B)Cr and Cu
C)Cs and Cl
D)Rb and Co
E)Fe and Co
A)Cu and C
B)Cr and Cu
C)Cs and Cl
D)Rb and Co
E)Fe and Co

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
62
Which of the following is the electron configuration of an excited state of an oxygen atom?
A)1s22s22p4
B)1s22s22p5
C)1s22s22p33s1
D)1s22s22p6
E)1s22s22p3
A)1s22s22p4
B)1s22s22p5
C)1s22s22p33s1
D)1s22s22p6
E)1s22s22p3

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
63
Transition metal elements have atoms or ions with partially filled
A)s subshells.
B)p subshells.
C)d subshells.
D)f subshells.
E)g subshells.
A)s subshells.
B)p subshells.
C)d subshells.
D)f subshells.
E)g subshells.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
64
Lanthanide (or rare earth elements)have atoms or ions with partially filled
A)s subshells.
B)p subshells.
C)d subshells.
D)f subshells.
E)g subshells.
A)s subshells.
B)p subshells.
C)d subshells.
D)f subshells.
E)g subshells.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
65
A ground-state chromium atom has how many unpaired electrons?
A)1
B)2
C)4
D)5
E)6
A)1
B)2
C)4
D)5
E)6

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
66
Which of the following is the electron configuration of an excited state of an iron atom?
A)[Ar]4s23d7
B)[Ar]4s23d6
C)[Ar]4s23d8
D)[Ar]4s13d7
E)[Ar]4s13d5
A)[Ar]4s23d7
B)[Ar]4s23d6
C)[Ar]4s23d8
D)[Ar]4s13d7
E)[Ar]4s13d5

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
67
How many electrons in a ground-state tellurium atom are in orbitals labeled by l = 1?
A)4
B)10
C)12
D)16
E)22
A)4
B)10
C)12
D)16
E)22

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
68
Which of the following ground-state atoms is diamagnetic?
A)Ca
B)As
C)Cu
D)Fe
E)none of these
A)Ca
B)As
C)Cu
D)Fe
E)none of these

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
69
How many electrons in a ground-state cadmium atom are in orbitals labeled by ml = -1?
A)2
B)10
C)12
D)18
E)36
A)2
B)10
C)12
D)18
E)36

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
70
A ground-state atom of vanadium has ___ unpaired electrons and is _____.
A)0, diamagnetic
B)2, diamagnetic
C)3, paramagnetic
D)5, paramagnetic
E)4, diamagnetic
A)0, diamagnetic
B)2, diamagnetic
C)3, paramagnetic
D)5, paramagnetic
E)4, diamagnetic

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
71
The electron in a hydrogen atom falls from an excited energy level to the ground state in two steps, causing the emission of photons with wavelengths of 1870 and 102.5 nm. What is the quantum number of the initial excited energy level from which the electron falls?
A)2
B)3
C)4
D)6
E)8
A)2
B)3
C)4
D)6
E)8

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
72
When the electron in a hydrogen atom falls from its first excited energy level to the ground state energy level, a photon with wavelength is emitted. A proton having this same wavelength would have a velocity of
A)3.87 m/s
B)5990 m/s
C)1.21 * 10-7 m/s
D)3.26 m/s
E)5.99 m/s
A)3.87 m/s
B)5990 m/s
C)1.21 * 10-7 m/s
D)3.26 m/s
E)5.99 m/s

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
73
The ground-state electron configuration of Cr, Mo, and Ag are exceptions to the Aufbau principle. Which of the following is the electron configuration for Mo?
A)[Kr]5s14d5
B)[Kr]5s24d4
C)[Xe]6s25d4
D)[Ar]4s24d4
E)[Kr]5s24d6
A)[Kr]5s14d5
B)[Kr]5s24d4
C)[Xe]6s25d4
D)[Ar]4s24d4
E)[Kr]5s24d6

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
74
Breaking the oxygen-oxygen bond in hydrogen peroxide requires 210 kJ/mol. What is the longest wavelength of light that can cause this bond to be broken?
A)5.7 * 10-4 m
B)9.5 * 10-31 m
C)2.8 * 10-7 m
D)9.5 * 10-28 m
E)5.7 * 10-7 m
A)5.7 * 10-4 m
B)9.5 * 10-31 m
C)2.8 * 10-7 m
D)9.5 * 10-28 m
E)5.7 * 10-7 m

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
75
Which of the following atoms is paramagnetic both in its ground state and in all of its excited states?
A)C
B)N
C)O
D)Ti
E)Cr
A)C
B)N
C)O
D)Ti
E)Cr

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
76
Which of the following is diamagnetic both in its ground state and in all of its excited states?
A)Mg
B)Ne
C)Cu
D)Zn
E)none of these
A)Mg
B)Ne
C)Cu
D)Zn
E)none of these

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
77
When the electron in a hydrogen atom falls from the n = 3 excited energy level to the ground state energy level, a photon with wavelength is emitted. An electron having this same wavelength would have a velocity of
A)7.10 * 103 m/s
B)2.93 * 106 m/s
C)2.93 * 103 m/s
D)7.10 m/s
E)3.00 * 108 m/s
A)7.10 * 103 m/s
B)2.93 * 106 m/s
C)2.93 * 103 m/s
D)7.10 m/s
E)3.00 * 108 m/s

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
78
Which of the following is the electron configuration of an excited state of a copper atom?
A)[Ar]4s23d9
B)[Ar]4s13d10
C)[Ar]4s13d8
D)[Ar]4s23d8
E)[Ar]4s03d10
A)[Ar]4s23d9
B)[Ar]4s13d10
C)[Ar]4s13d8
D)[Ar]4s23d8
E)[Ar]4s03d10

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
79
The electron in a hydrogen atom falls from an excited energy level to the ground state in two steps, causing the emission of photons with wavelengths of 2624 and 97.2 nm. What is the quantum number of the initial excited energy level from which the electron falls?
A)2
B)3
C)4
D)6
E)8
A)2
B)3
C)4
D)6
E)8

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck
80
A ground-state atom of iron has ___ unpaired electrons and is _____.
A)0, diamagnetic
B)6, diamagnetic
C)3, paramagnetic
D)5, paramagnetic
E)4, paramagnetic
A)0, diamagnetic
B)6, diamagnetic
C)3, paramagnetic
D)5, paramagnetic
E)4, paramagnetic

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 115 في هذه المجموعة.
فتح الحزمة
k this deck








