Deck 8: Basic Concepts of Chemical Bonding
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال

فتح الحزمة
قم بالتسجيل لفتح البطاقات في هذه المجموعة!
Unlock Deck
Unlock Deck
1/141
العب
ملء الشاشة (f)
Deck 8: Basic Concepts of Chemical Bonding
1
The electron configuration [Kr]4d10 represents __________.
A)Sr+2
B)Sn+2
C)Te+2
D)Ag+1
E)Rb+1
A)Sr+2
B)Sn+2
C)Te+2
D)Ag+1
E)Rb+1
Ag+1
2
The bond length in an HI molecule is 1.61 Å and the measured dipole moment is 0.44 D. What is the magnitude (in units of e)of the negative charge on I in HI? (1 debye = 3.34 × 10-30 coulomb-meters; e=1.6 × 10-19 coulombs)
A)1.6 × 10-19
B)0.057
C)9.1
D)1
E)0.22
A)1.6 × 10-19
B)0.057
C)9.1
D)1
E)0.22
0.057
3
In which of the molecules below is the carbon-carbon distance the shortest?
A)H2C-CH2
B)H-C≡C-H
C)H3C-CH3
D)H2C-C-CH2
E)H3C-CH2-C H3
A)H2C-CH2
B)H-C≡C-H
C)H3C-CH3
D)H2C-C-CH2
E)H3C-CH2-C H3
H-C≡C-H
4
Of the atoms below, __________ is the most electronegative.
A)Si
B)Cl
C)Rb
D)Ca
E)S
A)Si
B)Cl
C)Rb
D)Ca
E)S

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
5
There are __________ valence electrons in the Lewis structure of CH3CH2Cl.
A)14
B)12
C)18
D)20
E)10
A)14
B)12
C)18
D)20
E)10

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
6
Which energy change corresponds to the first ionization energy of potassium?
A)2
B)5
C)4
D)3
E)6
A)2
B)5
C)4
D)3
E)6

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
7
Which energy change corresponds to the electron affinity of fluorine?
A)2
B)5
C)4
D)1
E)6
A)2
B)5
C)4
D)1
E)6

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
8
Which of the following does not have eight valence electrons?
A)Ca+
B)Rb+
C)Xe
D)Br-
E)All of the above have eight valence electrons.
A)Ca+
B)Rb+
C)Xe
D)Br-
E)All of the above have eight valence electrons.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
9
Using the Born-Haber cycle, the ΔHf° of KBr is equal to __________.
A)ΔHf°[K (g)] + ΔHf°[Br (g)] + Il(K)+ E(Br)+ ΔHlattice
B)ΔHf°[K (g)] - ΔHf°[Br (g)] - Il(K)- E(Br)- ΔHlattice
C)ΔHf°[K (g)] - ΔHf°[Br (g)] + Il(K)- E(Br)+ ΔHlattice
D)ΔHf°[K (g)] + ΔHf°[Br (g)] - Il - E(Br)+ ΔHlattice
E)ΔHf°[K (g)] + ΔHf°[Br (g)] + Il(K)+ E(Br)- ΔHlattice
A)ΔHf°[K (g)] + ΔHf°[Br (g)] + Il(K)+ E(Br)+ ΔHlattice
B)ΔHf°[K (g)] - ΔHf°[Br (g)] - Il(K)- E(Br)- ΔHlattice
C)ΔHf°[K (g)] - ΔHf°[Br (g)] + Il(K)- E(Br)+ ΔHlattice
D)ΔHf°[K (g)] + ΔHf°[Br (g)] - Il - E(Br)+ ΔHlattice
E)ΔHf°[K (g)] + ΔHf°[Br (g)] + Il(K)+ E(Br)- ΔHlattice

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
10
The type of compound that is most likely to contain a covalent bond is __________.
A)one that is composed of a metal from the far left of the periodic table and a nonmetal from the far right of the periodic table
B)a solid metal
C)one that is composed of only nonmetals
D)held together by the electrostatic forces between oppositely charged ions
E)There is no general rule to predict covalency in bonds.
A)one that is composed of a metal from the far left of the periodic table and a nonmetal from the far right of the periodic table
B)a solid metal
C)one that is composed of only nonmetals
D)held together by the electrostatic forces between oppositely charged ions
E)There is no general rule to predict covalency in bonds.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
11
Which of the following has eight valence electrons?
A)Ti4+
B)Kr
C)Cl-
D)Na+
E)all of the above
A)Ti4+
B)Kr
C)Cl-
D)Na+
E)all of the above

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
12
Fe+2 ions are represented by __________.
A)[Ar]3d1
B)[Ar]3d4
C)[Ar]3d6
D)[Ar]3d104s1
E)[Ar]3d3
A)[Ar]3d1
B)[Ar]3d4
C)[Ar]3d6
D)[Ar]3d104s1
E)[Ar]3d3

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
13
The Lewis structure of N2H2 shows __________.
A)a nitrogen-nitrogen triple bond
B)a nitrogen-nitrogen single bond
C)each nitrogen has one nonbonding electron pair
D)each nitrogen has two nonbonding electron pairs
E)each hydrogen has one nonbonding electron pair
A)a nitrogen-nitrogen triple bond
B)a nitrogen-nitrogen single bond
C)each nitrogen has one nonbonding electron pair
D)each nitrogen has two nonbonding electron pairs
E)each hydrogen has one nonbonding electron pair

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
14
In ionic bond formation, the lattice energy of ions ________ as the magnitude of the ion charges _______ and the radii __________.
A)increases, decrease, increase
B)increases, increase, increase
C)decreases, increase, increase
D)increases, increase, decrease
E)increases, decrease, decrease
A)increases, decrease, increase
B)increases, increase, increase
C)decreases, increase, increase
D)increases, increase, decrease
E)increases, decrease, decrease

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
15
There are __________ valence electrons in the Lewis structure of CH3OCH2CH3.
A)18
B)20
C)26
D)32
E)36
A)18
B)20
C)26
D)32
E)36

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
16
Of the molecules below, the bond in __________ is the most polar.
A)HBr
B)HI
C)HCl
D)HF
E)H2
A)HBr
B)HI
C)HCl
D)HF
E)H2

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
17
Of the ions below, only __________ has a noble gas electron configuration.
A)S3-
B)O2+
C)I+
D)K-
E)Cl-
A)S3-
B)O2+
C)I+
D)K-
E)Cl-

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
18
Which of the following has the bonds correctly arranged in order of increasing polarity?
A)Be-F, Mg-F, N-F, O-F
B)O-F, N-F, Be-F, Mg-F
C)O-F, Be-F, Mg-F, N-F
D)N-F, Be-F, Mg-F, O-F
E)Mg-F, Be-F, N-F, O-F
A)Be-F, Mg-F, N-F, O-F
B)O-F, N-F, Be-F, Mg-F
C)O-F, Be-F, Mg-F, N-F
D)N-F, Be-F, Mg-F, O-F
E)Mg-F, Be-F, N-F, O-F

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
19
Which ion below has a noble gas electron configuration?
A)Li2+
B)Be2+
C)B2+
D)C2+
E)N2-
A)Li2+
B)Be2+
C)B2+
D)C2+
E)N2-

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
20
Lattice energy is __________.
A)the energy required to convert a mole of ionic solid into its constituent ions in the gas phase
B)the energy given off when gaseous ions combine to form one mole of an ionic solid
C)the energy required to produce one mole of an ionic compound from its constituent elements in their standard states
D)the sum of ionization energies of the components in an ionic solid
E)the sum of electron affinities of the components in an ionic solid
A)the energy required to convert a mole of ionic solid into its constituent ions in the gas phase
B)the energy given off when gaseous ions combine to form one mole of an ionic solid
C)the energy required to produce one mole of an ionic compound from its constituent elements in their standard states
D)the sum of ionization energies of the components in an ionic solid
E)the sum of electron affinities of the components in an ionic solid

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
21
In which of the ions do all X-O bonds (X indicates the central atom)have the same length?
A)none
B)all
C)(i)and (ii)
D)(iii)and (v)
E)(iii), (iv), and (v)
A)none
B)all
C)(i)and (ii)
D)(iii)and (v)
E)(iii), (iv), and (v)

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
22
The Lewis structure of the COH32- ion is __________.
A)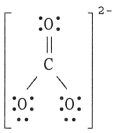
B)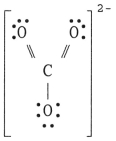
C)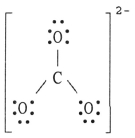
D)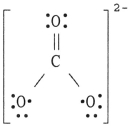
E)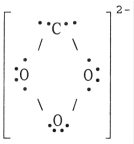
A)

B)

C)

D)

E)


فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
23
A valid Lewis structure of __________ cannot be drawn without violating the octet rule.
A)ClF3
B)PCl3
C)SO3
D)CCl4
E)CO2
A)ClF3
B)PCl3
C)SO3
D)CCl4
E)CO2

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
24
For resonance forms of a molecule or ion, __________.
A)one always corresponds to the observed structure
B)all the resonance structures are observed in various proportions
C)the observed structure is an average of the resonance forms
D)the same atoms need not be bonded to each other in all resonance forms
E)there cannot be more than two resonance structures for a given species
A)one always corresponds to the observed structure
B)all the resonance structures are observed in various proportions
C)the observed structure is an average of the resonance forms
D)the same atoms need not be bonded to each other in all resonance forms
E)there cannot be more than two resonance structures for a given species

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
25
A valid Lewis structure of __________ cannot be drawn without violating the octet rule.
A)PO43-
B)SiF4
C)CF4
D)SeF4
E)NF3
A)PO43-
B)SiF4
C)CF4
D)SeF4
E)NF3

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
26
The oxidation number of phosphorus in PF3 is __________.
A)-2
B)+1
C)+3
D)+2
E)-3
A)-2
B)+1
C)+3
D)+2
E)-3

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
27
In the nitrite ion (NO2-), __________.
A)both bonds are single bonds
B)both bonds are double bonds
C)one bond is a double bond and the other is a single bond
D)both bonds are the same
E)there are 20 valence electrons
A)both bonds are single bonds
B)both bonds are double bonds
C)one bond is a double bond and the other is a single bond
D)both bonds are the same
E)there are 20 valence electrons

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
28
To convert from one resonance structure to another, __________.
A)only atoms can be moved
B)electrons and atoms can both be moved
C)only electrons can be moved
D)neither electrons nor atoms can be moved
E)electrons must be added
A)only atoms can be moved
B)electrons and atoms can both be moved
C)only electrons can be moved
D)neither electrons nor atoms can be moved
E)electrons must be added

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
29
A valid Lewis structure of __________ cannot be drawn without violating the octet rule.
A)NF3
B)BeH2
C)SO2
D)CF4
E)SO32-
A)NF3
B)BeH2
C)SO2
D)CF4
E)SO32-

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
30
A valid Lewis structure of __________ cannot be drawn without violating the octet rule.
A)NF3
B)IF3
C)PF3
D)SbF3
E)SO42-
A)NF3
B)IF3
C)PF3
D)SbF3
E)SO42-

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
31
In the Lewis symbol for a sulfur atom, there are __________ paired and __________ unpaired electrons.
A)2, 2
B)4, 2
C)2, 4
D)0, 6
E)5, 1
A)2, 2
B)4, 2
C)2, 4
D)0, 6
E)5, 1

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
32
Resonance structures differ by __________.
A)number and placement of electrons
B)number of electrons only
C)placement of atoms only
D)number of atoms only
E)placement of electrons only
A)number and placement of electrons
B)number of electrons only
C)placement of atoms only
D)number of atoms only
E)placement of electrons only

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
33
Why don't we draw double bonds between the Be atom and the Cl atoms in BeCl2?
A)That would give positive formal charges to the chlorine atoms and a negative formal charge to the beryllium atom.
B)There aren't enough electrons.
C)That would result in more than eight electrons around beryllium.
D)That would result in more than eight electrons around each chlorine atom.
E)That would result in the formal charges not adding up to zero.
A)That would give positive formal charges to the chlorine atoms and a negative formal charge to the beryllium atom.
B)There aren't enough electrons.
C)That would result in more than eight electrons around beryllium.
D)That would result in more than eight electrons around each chlorine atom.
E)That would result in the formal charges not adding up to zero.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
34
There can be four equivalent best resonance structures of __________.
A)(i)
B)(ii)
C)(iii)
D)(iv)
E)(v)
A)(i)
B)(ii)
C)(iii)
D)(iv)
E)(v)

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
35
Which of the following does not have eight valence electrons?
A)Cl-
B)Xe
C)Ti+4
D)Rb+1
E)Sr+1
A)Cl-
B)Xe
C)Ti+4
D)Rb+1
E)Sr+1

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
36
The central atom in __________ violates the octet rule.
A)NH3
B)SeF2
C)BF3
D)AsF3
E)CF4
A)NH3
B)SeF2
C)BF3
D)AsF3
E)CF4

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
37
Based on the octet rule, boron will most likely form a __________ ion.
A)B3-
B)B1+
C)B3+
D)B2+
E)B2-
A)B3-
B)B1+
C)B3+
D)B2+
E)B2-

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
38
The central atom in __________ does not violate the octet rule.
A)SF4
B)KrF2
C)CF4
D)XeF4
E)ICl4-
A)SF4
B)KrF2
C)CF4
D)XeF4
E)ICl4-

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
39
A valid Lewis structure of __________ cannot be drawn without violating the octet rule.
A)NI3
B)SO2
C)ICl5
D)SiF4
E)CO2
A)NI3
B)SO2
C)ICl5
D)SiF4
E)CO2

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
40
The oxidation number of iron in Fe2O3 is __________.
A)-2
B)+1
C)+3
D)+2
E)-3
A)-2
B)+1
C)+3
D)+2
E)-3

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
41
The electron configuration of the phosphide ion (P3-)is __________.
A)[Ne]3s2
B)[Ne]3s23Pl
C)[Ne]3s23P3
D)[Ne]3P2
E)[Ne]3s23P6
A)[Ne]3s2
B)[Ne]3s23Pl
C)[Ne]3s23P3
D)[Ne]3P2
E)[Ne]3s23P6

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
42
Which of the following would have to lose three electrons in order to achieve a noble gas electron configuration? Si Mg Al Cl P
A)Si, P
B)Al
C)P
D)Cl
E)Mg, Al, P
A)Si, P
B)Al
C)P
D)Cl
E)Mg, Al, P

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
43
Based on the octet rule, phosphorus most likely forms a __________ ion.
A)P3+
B)P3-
C)P5+
D)P5-
E)P+
A)P3+
B)P3-
C)P5+
D)P5-
E)P+

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
44
Bond enthalpy is __________.
A)always positive
B)always negative
C)sometimes positive, sometimes negative
D)always zero
E)unpredictable
A)always positive
B)always negative
C)sometimes positive, sometimes negative
D)always zero
E)unpredictable

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
45
As the number of covalent bonds between two atoms increases, the distance between the atoms __________ and the strength of the bond between them __________.
A)increases, increases
B)decreases, decreases
C)increases, decreases
D)decreases, increases
E)is unpredictable
A)increases, increases
B)decreases, decreases
C)increases, decreases
D)decreases, increases
E)is unpredictable

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
46
Based on the octet rule, aluminum most likely forms an __________ ion.
A)Al3+
B)Al4+
C)Al4-
D)Al+
E)Al-
A)Al3+
B)Al4+
C)Al4-
D)Al+
E)Al-

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
47
Which of the following would have to lose two electrons in order to achieve a noble gas electron configuration? O Sr Na Se Br
A)O, Se
B)Sr
C)Na
D)Br
E)Sr, O, Se
A)O, Se
B)Sr
C)Na
D)Br
E)Sr, O, Se

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
48
The halogens, alkali metals, and alkaline earth metals have __________ valence electrons, respectively.
A)7, 4, and 6
B)1, 5, and 7
C)8, 2, and 3
D)7, 1, and 2
E)2, 7, and 4
A)7, 4, and 6
B)1, 5, and 7
C)8, 2, and 3
D)7, 1, and 2
E)2, 7, and 4

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
49
Dynamite __________.
A)was invented by Alfred Nobel
B)is made of nitroglycerine and an absorbent such as diatomaceous earth
C)is a much safer explosive than pure nitroglycerine
D)is an explosive
E)all of the above
A)was invented by Alfred Nobel
B)is made of nitroglycerine and an absorbent such as diatomaceous earth
C)is a much safer explosive than pure nitroglycerine
D)is an explosive
E)all of the above

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
50
Of the bonds C-N, C-N, and C≡N, the C-N bond is __________.
A)strongest/shortest
B)strongest/longest
C)weakest/shortest
D)weakest/longest
E)intermediate in both strength and length
A)strongest/shortest
B)strongest/longest
C)weakest/shortest
D)weakest/longest
E)intermediate in both strength and length

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
51
Dynamite consists of nitroglycerine mixed with __________.
A)potassium nitrate
B)damp KOH
C)TNT
D)diatomaceous earth or cellulose
E)solid carbon
A)potassium nitrate
B)damp KOH
C)TNT
D)diatomaceous earth or cellulose
E)solid carbon

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
52
Based on the octet rule, iodine most likely forms an __________ ion.
A)I2+
B)I4+
C)I4-
D)I+
E)I-
A)I2+
B)I4+
C)I4-
D)I+
E)I-

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
53
The only noble gas without eight valence electrons is __________.
A)Ar
B)Ne
C)He
D)Kr
E)All noble gases have eight valence electrons.
A)Ar
B)Ne
C)He
D)Kr
E)All noble gases have eight valence electrons.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
54
Most explosives are compounds that decompose rapidly to produce __________ products and a great deal of __________.
A)gaseous, gases
B)liquid, heat
C)soluble, heat
D)solid, gas
E)gaseous, heat
A)gaseous, gases
B)liquid, heat
C)soluble, heat
D)solid, gas
E)gaseous, heat

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
55
Of the bonds C-C, C-C, and C≡C, the C-C bond is __________.
A)strongest/shortest
B)strongest/longest
C)weakest/longest
D)weakest/shortest
E)intermediate in both strength and length
A)strongest/shortest
B)strongest/longest
C)weakest/longest
D)weakest/shortest
E)intermediate in both strength and length

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
56
Given that the average bond energies for C-H and C-Br bonds are 413 and 276 kJ/mol, respectively, the heat of atomization of bromoform (CHBr3)is __________ kJ/mol.
A)1241
B)689
C)-689
D)1378
E)-1378
A)1241
B)689
C)-689
D)1378
E)-1378

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
57
The electron configuration of the sulfide ion (S2-)is __________.
A)[Ne]3s2
B)[Ne]3s23Pl
C)[Ne]3s23P4
D)[Ne]3P2
E)[Ne]3s23P6
A)[Ne]3s2
B)[Ne]3s23Pl
C)[Ne]3s23P4
D)[Ne]3P2
E)[Ne]3s23P6

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
58
Which atom can accommodate an octet of electrons, but doesn't necessarily have to accommodate an octet?
A)N
B)C
C)H
D)O
E)B
A)N
B)C
C)H
D)O
E)B

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
59
Based on the octet rule, magnesium most likely forms a __________ ion.
A)Mg2+
B)Mg2-
C)Mg6-
D)Mg6+
E)Mg-
A)Mg2+
B)Mg2-
C)Mg6-
D)Mg6+
E)Mg-

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
60
Of the possible bonds between carbon atoms (single, double, and triple), __________.
A)a triple bond is longer than a single bond
B)a double bond is stronger than a triple bond
C)a single bond is stronger than a triple bond
D)a double bond is longer than a triple bond
E)a single bond is stronger than a double bond
A)a triple bond is longer than a single bond
B)a double bond is stronger than a triple bond
C)a single bond is stronger than a triple bond
D)a double bond is longer than a triple bond
E)a single bond is stronger than a double bond

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
61
For a given arrangement of ions, the lattice energy increases as ionic radius __________ and as ionic charge __________.
A)decreases, increases
B)increases, decreases
C)increases, increases
D)decreases, decreases
E)This cannot be predicted.
A)decreases, increases
B)increases, decreases
C)increases, increases
D)decreases, decreases
E)This cannot be predicted.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
62
Which of the following would have to gain two electrons in order to achieve a noble gas electron configuration? O Sr Na Se Br
A)Br
B)Sr
C)Na
D)O, Se
E)Sr, O, Se
A)Br
B)Sr
C)Na
D)O, Se
E)Sr, O, Se

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
63
For a given arrangement of ions, the lattice energy decreases as ionic radius __________ and as ionic charge __________.
A)decreases, increases
B)increases, decreases
C)increases, increases
D)decreases, decreases
E)This cannot be predicted.
A)decreases, increases
B)increases, decreases
C)increases, increases
D)decreases, decreases
E)This cannot be predicted.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
64
What is the maximum number of double bonds that a carbon atom can form?
A)4
B)1
C)0
D)2
E)3
A)4
B)1
C)0
D)2
E)3

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
65
What is the maximum number of double bonds that a hydrogen atom can form?
A)0
B)1
C)2
D)3
E)4
A)0
B)1
C)2
D)3
E)4

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
66
What is the electron configuration for the Fe3+ ion?
A)[Ar]4s13d6
B)[Ar]4s03d7
C)[Ar]4s03d5
D)[Ar]4s23d9
E)[Ne]3s23p10
A)[Ar]4s13d6
B)[Ar]4s03d7
C)[Ar]4s03d5
D)[Ar]4s23d9
E)[Ne]3s23p10

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
67
The electron configuration of the P3- ion is __________.
A)[Ar]3s23P6
B)[Ar]3s23P2
C)[Ne]3s23P6
D)[Ne]3s23P2
E)[Kr]3s23P-6
A)[Ar]3s23P6
B)[Ar]3s23P2
C)[Ne]3s23P6
D)[Ne]3s23P2
E)[Kr]3s23P-6

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
68
What is the electron configuration for the Co2+ ion?
A)[Ar]4s13d6
B)[Ar]3d7
C)[Ar]3d5
D)[Ar]4s23d9
E)[Ne]3s23p10
A)[Ar]4s13d6
B)[Ar]3d7
C)[Ar]3d5
D)[Ar]4s23d9
E)[Ne]3s23p10

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
69
Determining lattice energy from Born-Haber cycle data requires the use of __________.
A)the octet rule
B)Coulomb's law
C)Periodic law
D)Hess's law
E)Avogadro's number
A)the octet rule
B)Coulomb's law
C)Periodic law
D)Hess's law
E)Avogadro's number

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
70
How many hydrogen atoms must bond to silicon to give it an octet of valence electrons?
A)1
B)2
C)3
D)4
E)5
A)1
B)2
C)3
D)4
E)5

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
71
What species has the electron configuration [Ar]3d2?
A)Mn2+
B)Cr2+
C)V3+
D)Fe3+
E)K+
A)Mn2+
B)Cr2+
C)V3+
D)Fe3+
E)K+

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
72
The electron configuration of the S2- ion is __________.
A)[Ar]3s23P6
B)[Ar]3s23P2
C)[Ne]3s23P2
D)[Ne]3s23P6
E)[Kr]3s23P-6
A)[Ar]3s23P6
B)[Ar]3s23P2
C)[Ne]3s23P2
D)[Ne]3s23P6
E)[Kr]3s23P-6

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
73
What is the maximum number of triple bonds that a carbon atom can form?
A)4
B)1
C)0
D)2
E)3
A)4
B)1
C)0
D)2
E)3

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
74
What species has the electron configuration [Ar]3d4?
A)Mn2+
B)Cr2+
C)V3+
D)Fe3+
E)K+
A)Mn2+
B)Cr2+
C)V3+
D)Fe3+
E)K+

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
75
Elements from opposite sides of the periodic table tend to form __________.
A)covalent compounds
B)ionic compounds
C)compounds that are gaseous at room temperature
D)homonuclear diatomic compounds
E)covalent compounds that are gaseous at room temperature
A)covalent compounds
B)ionic compounds
C)compounds that are gaseous at room temperature
D)homonuclear diatomic compounds
E)covalent compounds that are gaseous at room temperature

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
76
A __________ covalent bond between the same two atoms is the longest.
A)single
B)double
C)triple
D)They are all the same length.
E)strong
A)single
B)double
C)triple
D)They are all the same length.
E)strong

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
77
The formula of palladium(IV)sulfide is __________.
A)Pd2S4
B)PdS4
C)Pd4S
D)PdS2
E)Pd2S2
A)Pd2S4
B)PdS4
C)Pd4S
D)PdS2
E)Pd2S2

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
78
A double bond consists of __________ pairs of electrons shared between two atoms.
A)1
B)2
C)3
D)4
E)6
A)1
B)2
C)3
D)4
E)6

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
79
A triple bond consists of __________ pairs of electrons shared between two atoms.
A)1
B)2
C)3
D)4
E)6
A)1
B)2
C)3
D)4
E)6

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck
80
What is the electron configuration for the Fe2+ ion?
A)[Ar]4s03d6
B)[Ar]4s23d4
C)[Ar]4s03d8
D)[Ar]4s23d8
E)[Ar]4s63d2
A)[Ar]4s03d6
B)[Ar]4s23d4
C)[Ar]4s03d8
D)[Ar]4s23d8
E)[Ar]4s63d2

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 141 في هذه المجموعة.
فتح الحزمة
k this deck








