Deck 3: Chemical Bonds
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال
سؤال

فتح الحزمة
قم بالتسجيل لفتح البطاقات في هذه المجموعة!
Unlock Deck
Unlock Deck
1/83
العب
ملء الشاشة (f)
Deck 3: Chemical Bonds
1
Which of the following has the lowest lattice energy?
A)KCl
B)LiCl
C)KBr
D)NaCl
E)KI
A)KCl
B)LiCl
C)KBr
D)NaCl
E)KI
KI
2
How many lone pairs of electrons are found in the Lewis structure of urea,(NH2)2CO?
A)2
B)3
C)6
D)4
E)8
A)2
B)3
C)6
D)4
E)8
4
3
If 491 kJ.mol-1 is released in the reaction Na+(g)+ Cl-(g) Na+Cl-(g),what is the energy change for the reaction Na(g)+ Cl(g) Na+Cl-(g)? (Hint: See the discussion in the text and apply Hess's Law.)
-346 kJ.mol-1
4
Metals rarely lose electrons in chemical reactions because
A)their electron affinities are too high.
B)their ionic radii become too small.
C)their ionization energies are too small.
D)their size is too small.
E)their ionization energies are too high.
A)their electron affinities are too high.
B)their ionic radii become too small.
C)their ionization energies are too small.
D)their size is too small.
E)their ionization energies are too high.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
5
How many lone pairs of electrons are found in the Lewis structure of the interhalogen compound ICl3?
A)10
B)4
C)8
D)6
E)7
A)10
B)4
C)8
D)6
E)7

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
6
Use the expression for the Coulomb potential energy to calculate the energy for formation of 1 mole of rubidium chloride ion-pairs,that is,the energy change for the following reaction:
Rb+(g)+ Cl-(g) Rb+Cl-(g)
Use r12 = 330 pm.
Rb+(g)+ Cl-(g) Rb+Cl-(g)
Use r12 = 330 pm.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
7
For the ground-state ion Pb2+,what type of orbital do the electrons with highest energy reside in?
A)6p
B)5p
C)4f
D)6s
E)5d
A)6p
B)5p
C)4f
D)6s
E)5d

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
8
Predict the electronic configuration in the oxide ion in CaO.
A)[He]2s22p6 or [Ne]
B)[He]2s22p5
C)[He]2s22p63s2
D)[Ne]3s13p3
E)[Ne]3s23p3
A)[He]2s22p6 or [Ne]
B)[He]2s22p5
C)[He]2s22p63s2
D)[Ne]3s13p3
E)[Ne]3s23p3

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
9
Which of the following has the highest lattice energy?
A)NaCl
B)KI
C)MgO
D)BaO
E)CaO
A)NaCl
B)KI
C)MgO
D)BaO
E)CaO

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
10
All the following elements exist as diatomic gases at room temperature and atmospheric pressure except
A)H.
B)Ar.
C)N.
D)Cl.
E)O.
A)H.
B)Ar.
C)N.
D)Cl.
E)O.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
11
An element,E,has the electronic configuration [Ne] 3s23p1.Write the formula of its compound with sulfate.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
12
The Madelung constant is different for all crystals.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
13
If 346 kJ.mol-1 is released in the reaction Na(g)+ Cl(g) Na+Cl-(g),is the energy change for the reaction Na+Cl-(g) NaCl(s)endothermic or exothermic?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
14
For the ground-state ion Sn4+,what type of orbital do the electrons with highest energy reside in?
A)4p
B)5p
C)4f
D)4d
E)5s
A)4p
B)5p
C)4f
D)4d
E)5s

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
15
For the ground-state ion Bi3+,what type of orbital do the electrons with highest energy reside in?
A)5d
B)6s
C)4f
D)5p
E)6p
A)5d
B)6s
C)4f
D)5p
E)6p

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
16
Because of the octet rule,the gaseous O2- ion is stable.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
17
Which of the following metal ions has the ground-state electron configuration [Ar]3d6?
A)Ni3+
B)Fe2+
C)Mn2+
D)Cu+
E)Ca2+
A)Ni3+
B)Fe2+
C)Mn2+
D)Cu+
E)Ca2+

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
18
Which of the following has the highest melting point?
A)KF
B)KI
C)RbF
D)KBr
E)KCl
A)KF
B)KI
C)RbF
D)KBr
E)KCl

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
19
For the ground-state ion I-,what type of orbital do the electrons with highest energy reside in?
A)4d
B)6s
C)5p
D)5d
E)5s
A)4d
B)6s
C)5p
D)5d
E)5s

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
20
Use the expression for the Coulomb potential energy to calculate the energy for formation of 1 mole of sodium chloride ion-pairs,that is,the energy change for the following reaction:
Na+(g)+ Cl-(g) Na+Cl-(g)
Use r12 = 283 pm.
Na+(g)+ Cl-(g) Na+Cl-(g)
Use r12 = 283 pm.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
21
Which of the following species are radicals?
A)CH2O
B)HCN
C)HclO
D)ClONO2
E)ClO
A)CH2O
B)HCN
C)HclO
D)ClONO2
E)ClO

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
22
Predict the N-O bond lengths in NO2-,given the N-O and N=O bond lengths of 140 and 120 pm,respectively.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
23
How many electrons are in the expanded valence in XeO4?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
24
Which of the following species has bonds with the most ionic character?
A)SiO2
B)PCl3
C)P4O10
D)CO2
E)NO2
A)SiO2
B)PCl3
C)P4O10
D)CO2
E)NO2

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
25
How many lone pairs of electrons are found in the Lewis structure of hydrazine,H2NNH2?
A)8
B)4
C)1
D)0
E)2
A)8
B)4
C)1
D)0
E)2

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
26
In the "best" Lewis structure of XeO4,there are two double bonds and the formal charge on Xe is zero.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
27
Which of the following species are radicals?
A)CO2
B)HNO3
C)NO2
D)NO3-
E)HNO3
A)CO2
B)HNO3
C)NO2
D)NO3-
E)HNO3

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
28
For dinitrogen monoxide,the arrangement of the atoms is N-N-O.In the Lewis structure with a single bond between NN and a triple bond between NO,the formal charges on N,N,and O,respectively,are
A)(-1,+1,0.)
B)0,0,0.
C)0,+1,-1.
D)0,-1,+1.
E)(-2,+1,+1.)
A)(-1,+1,0.)
B)0,0,0.
C)0,+1,-1.
D)0,-1,+1.
E)(-2,+1,+1.)

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
29
Why are the N-O bond lengths in NO3- the same?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
30
Consider the following equilibrium:
S2O42-(aq)↔ 2SO2-(aq)
K ~ 10-9
Write a Lewis structure for each species.
S2O42-(aq)↔ 2SO2-(aq)
K ~ 10-9
Write a Lewis structure for each species.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
31
How many electrons are in the expanded valence in I3-?
A)12
B)6
C)10
D)14
E)8
A)12
B)6
C)10
D)14
E)8

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
32
Draw the Lewis structure of the formate ion and indicate whether resonance forms are possible.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
33
For dinitrogen monoxide,the arrangement of the atoms is N-N-O.In the Lewis structure with a double bond between NN and NO,the formal charges on N,N,and O,respectively,are
A)0,-1,+1.
B)(-1,+1,0.)
C)(0,+1,-1.)
D)0,0,0.
E)(-2,+1,+1.)
A)0,-1,+1.
B)(-1,+1,0.)
C)(0,+1,-1.)
D)0,0,0.
E)(-2,+1,+1.)

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
34
In the most plausible Lewis structure of XeOF2,there are
A)2 single bonds,1 double bond,and 1 lone pair of electrons around Xe.
B)3 single bonds and 1 lone pair of electrons around Xe.
C)2 single bonds,1 double bond,and 3 lone pairs of electrons around Xe.
D)2 single bonds,1 double bond,and 2 lone pairs of electrons around Xe.
E)3 single bonds and 2 lone pairs of electrons around Xe.
A)2 single bonds,1 double bond,and 1 lone pair of electrons around Xe.
B)3 single bonds and 1 lone pair of electrons around Xe.
C)2 single bonds,1 double bond,and 3 lone pairs of electrons around Xe.
D)2 single bonds,1 double bond,and 2 lone pairs of electrons around Xe.
E)3 single bonds and 2 lone pairs of electrons around Xe.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
35
Which of the following do not have resonance structures?
A)CH3CONH-
B)CH2COCH3-
C)H2CO
D)All have resonance structures.
A)CH3CONH-
B)CH2COCH3-
C)H2CO
D)All have resonance structures.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
36
Draw the "best" Lewis structures of hydrogen azide,HN1N2N3,and the azide ion,N1N2N3- .The subscripts are used for identification.For each,match the following bond lengths to the correct N-N bond.The bond lengths can be used more than once.



فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
37
How many electrons are in the expanded valence in XeOF2?
A)14
B)12
C)8
D)10
E)6
A)14
B)12
C)8
D)10
E)6

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
38
How many electrons are in the expanded valence in H2SO4?
A)12
B)14
C)8
D)6
E)10
A)12
B)14
C)8
D)6
E)10

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
39
Draw the Lewis structure of xenon difluoride and give the number of lone pairs electrons around the central atom.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
40
Write three Lewis structures for the cyanate ion,NCO-,where the arrangement of atoms is N-C-O.In the most plausible structure,
A)there is a triple bond between N and C.
B)there are two double bonds.
C)there is a triple bond between C and O.
D)the formal charge on O is +1.
E)the formal charge on N is -1.
A)there is a triple bond between N and C.
B)there are two double bonds.
C)there is a triple bond between C and O.
D)the formal charge on O is +1.
E)the formal charge on N is -1.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
41
Which of the following statements is true?
A)Atoms with high ionization energies and high electron affinities are highly electronegative.
B)Atoms with high ionization energies and high electron affinities have low electronegativities.
C)The electronegativity of an atom depends only on the value of the ionization energy of the atom.
D)Atoms with low ionization energies and low electron affinities have high electronegativities.
E)The electronegativity of an atom is defined as half the electron affinity of the atom.
A)Atoms with high ionization energies and high electron affinities are highly electronegative.
B)Atoms with high ionization energies and high electron affinities have low electronegativities.
C)The electronegativity of an atom depends only on the value of the ionization energy of the atom.
D)Atoms with low ionization energies and low electron affinities have high electronegativities.
E)The electronegativity of an atom is defined as half the electron affinity of the atom.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
42
Which of the following compounds contains the strongest bonds to hydrogen?
A)SiH4
B)CH4
C)HF
D)H2S
E)H2O
A)SiH4
B)CH4
C)HF
D)H2S
E)H2O

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
43
Estimate the CN bond length in urea,NH2CONH2.Given: covalent radii (pm)of C-,77; C=,67; N-,75; N=,60; O-,74; O=,60; H,37.
A)71 pm
B)127 pm
C)76 pm
D)152 pm
E)142 pm
A)71 pm
B)127 pm
C)76 pm
D)152 pm
E)142 pm

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
44
Use the bond enthalpies given to estimate the heat released when 1-bromobutene,CH3CH2CH=CH2,reacts with bromine to give CH3CH2CHBrCH2Br.Bond enthalpies (kJ.mol-1): C-H,412; C-C,348; C=C,612; C-Br,276; Br-Br,193.
A)181 kJ.mol-1
B)317 kJ.mol-1
C)288 kJ.mol-1
D)95 kJ.mol-1
E)507 kJ.mol-1
A)181 kJ.mol-1
B)317 kJ.mol-1
C)288 kJ.mol-1
D)95 kJ.mol-1
E)507 kJ.mol-1

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
45
Which of the following statements is true?
A)The electronegativity of an atom is defined as electron affinity of the atom.
B)The electronegativity of an atom depends only on the value of the ionization energy of the atom.
C)Atoms with high ionization energies and high electron affinities have low electronegativities.
D)Atoms with low ionization energies and low electron affinities have low electronegativities.
E)Atoms with low ionization energies and low electron affinities have high electronegativities.
A)The electronegativity of an atom is defined as electron affinity of the atom.
B)The electronegativity of an atom depends only on the value of the ionization energy of the atom.
C)Atoms with high ionization energies and high electron affinities have low electronegativities.
D)Atoms with low ionization energies and low electron affinities have low electronegativities.
E)Atoms with low ionization energies and low electron affinities have high electronegativities.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
46
If the following all crystallize in the same type of structure,which has the lowest lattice energy?
A)LiCl
B)NaI
C)NaCl
D)KCl
E)KI
A)LiCl
B)NaI
C)NaCl
D)KCl
E)KI

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
47
Use the bond enthalpies given to estimate the heat released when 2-methyl-1-propene,(CH3)2C=CH2,reacts with HBr to give (CH3)2CBrCH3.Bond enthalpies (kJ.mol-1): C-H,412; C-C,348; C=C,612; C-Br,276; H-Br,366.
A)58 kJ.mol-1
B)507 kJ.mol-1
C)317 kJ.mol-1
D)288 kJ.mol-1
E)181 kJ.mol-1
A)58 kJ.mol-1
B)507 kJ.mol-1
C)317 kJ.mol-1
D)288 kJ.mol-1
E)181 kJ.mol-1

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
48
Use the bond enthalpies given to estimate the heat released when ethene,CH2=CH2,reacts with HBr to give CH3CH2Br.Bond enthalpies (kJ.mol-1): C-H,412; C-C,348; C=C,612; C-Br,276; Br-Br,193; H-Br,366.
A)1036 kJ.mol-1
B)200 kJ.mol-1
C)470 kJ.mol-1
D)424 kJ.mol-1
E)58 kJ.mol-1
A)1036 kJ.mol-1
B)200 kJ.mol-1
C)470 kJ.mol-1
D)424 kJ.mol-1
E)58 kJ.mol-1

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
49
If the following all crystallize in the same type of structure,which has the highest lattice energy?
A)NaCl
B)NaF
C)KF
D)NaBr
E)NaI
A)NaCl
B)NaF
C)KF
D)NaBr
E)NaI

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
50
Write all possible Lewis structures of sulfur dioxide.Which structure is most feasible?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
51
Which of the following compounds contains the weakest bonds to hydrogen?
A)CH4
B)H2O
C)SiH4
D)HF
E)H2S
A)CH4
B)H2O
C)SiH4
D)HF
E)H2S

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
52
Estimate the CO bond length in acetone,CH3COCH3.Given: covalent radii (pm)of C-,77; C=,67; O-,74; O=,60; H,37.
A)75.5 pm
B)127 pm
C)63.5 pm
D)151 pm
E)137 pm
A)75.5 pm
B)127 pm
C)63.5 pm
D)151 pm
E)137 pm

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
53
Which of the compounds below has bonds with the least covalent character?
A)AgI
B)AgCl
C)AgF
D)AlCl3
E)BeCl2
A)AgI
B)AgCl
C)AgF
D)AlCl3
E)BeCl2

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
54
Which of the compounds below has bonds with the most covalent character?
A)CaO
B)Li2O
C)MgO
D)MgS
E)CaS
A)CaO
B)Li2O
C)MgO
D)MgS
E)CaS

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
55
Which of the following species has bonds with the most ionic character?
A)CO2
B)NO2
C)SnO2
D)P4O10
E)PCl3
A)CO2
B)NO2
C)SnO2
D)P4O10
E)PCl3

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
56
Which of the following compounds is the least stable?
A)CH4
B)SnH4
C)SiH4
D)GeH4
E)PbH4
A)CH4
B)SnH4
C)SiH4
D)GeH4
E)PbH4

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
57
If the following all crystallize in the same type of structure,which has the lowest lattice energy?
A)CaO
B)BaS
C)SrO
D)SrS
E)BaO
A)CaO
B)BaS
C)SrO
D)SrS
E)BaO

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
58
Use the bond enthalpies given to estimate the heat released when ethene,CH2=CH2,reacts with hydrogen to give CH3CH3.Bond enthalpies (kJ.mol-1): C-H,412; C-C,348; C=C,612; C-Br,276; H-H,436.
A)124 kJ.mol-1
B)342 kJ.mol-1
C)288 kJ.mol-1
D)148 kJ.mol-1
E)560 kJ.mol-1
A)124 kJ.mol-1
B)342 kJ.mol-1
C)288 kJ.mol-1
D)148 kJ.mol-1
E)560 kJ.mol-1

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
59
Which of the compounds below has bonds with the most covalent character?
A)NaCl
B)LiCl
C)CaCl2
D)BeCl2
E)MgCl2
A)NaCl
B)LiCl
C)CaCl2
D)BeCl2
E)MgCl2

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
60
If the following all crystallize in the same type of structure,which has the highest lattice energy?
A)LiCl
B)KF
C)KBr
D)KCl
E)LiF
A)LiCl
B)KF
C)KBr
D)KCl
E)LiF

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
61
How many resonance structures can be drawn for N2O?
A)0
B)3
C)2
D)1
A)0
B)3
C)2
D)1

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
62
There are three resonance structures of the sulfate ion.A resonance structure can be written where the formal charge on sulfur is 0.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
63
How many lone pairs of electrons are there in the Lewis structure of Al2Cl6?
A)24
B)12
C)4
D)16
A)24
B)12
C)4
D)16

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
64
The electronegativity of an element can be expressed as ½(I + Ea)where I is the ionization energy and Ea is the electron affinity.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
65
How many valence electrons are present in W4+?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
66
If dinitrogen oxide has a dipole moment,what is the arrangement of atoms?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
67
White phosphorus is composed of tetrahedral molecules of P4 in which each P atom is bonded to three others.In this molecule the formal charge on each P atom is ___.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
68
What is wrong with the following Lewis structure? 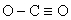
A)The valence electron count
B)The positioning of the carbon atom
C)The distribution of valence electrons
D)The charge on the carbon atom
E)The dipole of the molecule
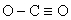
A)The valence electron count
B)The positioning of the carbon atom
C)The distribution of valence electrons
D)The charge on the carbon atom
E)The dipole of the molecule

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
69
What is the formal charge on the Xe atom in XeF4?
A)0
B)(-4)
C)+2
D)+4
A)0
B)(-4)
C)+2
D)+4

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
70
Of the following molecules,which has the strongest bonds?
A)H2O
B)H2Se
C)H2Te
D)H2S
A)H2O
B)H2Se
C)H2Te
D)H2S

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
71
The best Lewis structures of SO2 and O3 include expanded valence structures such as O=S=O and O=O=O.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
72
How many double bonds are present in the "best" resonance structure of the phosphate ion?
A)2
B)3
C)1
D)0
A)2
B)3
C)1
D)0

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
73
Match each of the following compounds with its lattice energy.
KI
LiF
MgF2
LiI
2961
1046
759
645 kJ/mol
KI
LiF
MgF2
LiI
2961
1046
759
645 kJ/mol

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
74
What is the electronic configuration of Ag?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
75
Which of the following is a radical?
A)BrO
B)CH3+
C)CH3-
D)BF4-
A)BrO
B)CH3+
C)CH3-
D)BF4-

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
76
Which of the following has resonance structures?
A)XeOF2
B)N2H4
C)CH3CONH-
D)H2CO
A)XeOF2
B)N2H4
C)CH3CONH-
D)H2CO

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
77
What is the formal charge of S in the molecule H2SO4?

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
78
Sulfur is more electronegative than oxygen.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
79
White phosphorus is composed of tetrahedral molecules of P4 in which every P atom is connected to three other P atoms.In the Lewis structure of P4,there are
A)3 bonding pairs and 4 lone pairs of electrons.
B)6 bonding pairs and 2 lone pairs of electrons.
C)5 bonding pairs and 4 lone pairs of electrons.
D)6 bonding pairs and no lone pairs of electrons.
E)6 bonding pairs and 4 lone pairs of electrons.
A)3 bonding pairs and 4 lone pairs of electrons.
B)6 bonding pairs and 2 lone pairs of electrons.
C)5 bonding pairs and 4 lone pairs of electrons.
D)6 bonding pairs and no lone pairs of electrons.
E)6 bonding pairs and 4 lone pairs of electrons.

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck
80
An element E has the electronic configuration 1s22s22p4.What is the formula of its compound with lithium?
A)LiE2
B)LiE
C)Li2E
D)Li4E
A)LiE2
B)LiE
C)Li2E
D)Li4E

فتح الحزمة
افتح القفل للوصول البطاقات البالغ عددها 83 في هذه المجموعة.
فتح الحزمة
k this deck








